用NA表示阿伏加德罗常数,下列说法中正确的是( )
| A.在常温常压下,11.2 L氯气所含的原子数目为NA |
| B.32 g氧气含的原子数目为NA |
| C.0.5mol的水含有的原子数是1.5 NA |
| D.2 L 0.1 mol·L-1 K2SO4溶液中离子总数约为1.4 NA |
化学用语是学习化学的重要工具,下列用来表示物质变化的化学用语中,正确的是()
A.电解饱和食盐水时,阳极的电极反 应式为:2CI—→Cl2↑+2e— 应式为:2CI—→Cl2↑+2e— |
| B.氢氧燃料电池的负极反应式:O2+2H2O+4e—→4OH— |
| C.粗铜精炼时,与电源正极相连的是纯铜,电极反应式为:Cu→Cu2++2e— |
| D.钢铁发生电化学腐蚀的正极反应式:Fe→Fe2++2e一 |
下列叙述正确的是()
A.Fe分别与氯气和稀盐酸反应所得氯化物相同
B.K、Al分别与不足量的稀硫酸反应所得溶液均呈中性
C.Li、Na、K的原子半径和密度随原子序数的增加而增大
D.C、P、S、Cl的最高价氧化物对应水化物的酸性逐渐增强
某地污水中含有Zn2+、Hg2+、Fe3+和Cu2+四种阳离子。甲、乙、丙三位同学设计的从该污水中回收金属铜的方案如下: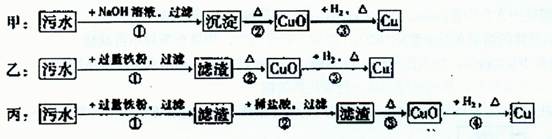
下列判断正确的是()
| A.甲方案中的反应涉及到置换、分解、化合、复分解四种反应类型 |
| B.乙方案中加过量铁粉可以将四种阳离子全部还原 |
| C.丙方案也发生环境污染 |
| D.三种实验方案中都能制得纯净铜 |
检验下列物质X是否已部分被氧化变质,所选用的试剂Y不正确的是()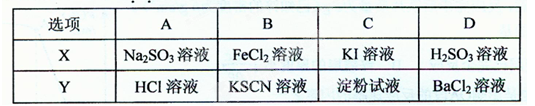
人类将在未来几十年内逐渐由“碳素燃料文明时代”过渡至“太阳能文明时代”(包括风能、生物质能等太阳能的转换形态),届时人们将适应“低碳经济”和“低碳生活”。下列说法不正确的是()
| A.煤、石油和天然气都属于碳素燃料 |
| B.发展太阳能经济有助于减缓温室效应 |
| C.太阳能电池可将太阳能直接转化为电能 |
| D.目前正在研究的菠菜蛋白质“发电”不属于太阳能文明 |