在不同温度下,水达到电离平衡时c(H+)与c(OH—)的关系如图4所示,下列说法中正确的是
| A.100℃时,pH=12的NaOH溶液和pH=2的H2SO4溶液恰好中和,所得溶液的pH等于7 |
| B.25℃时,0.2 mol/L Ba(OH)2溶液和0.2 mol/L HCl溶液等体积混合,所得溶液的pH等于7 |
| C.25℃时, 0.2 mol/L NaOH溶液与0.2 mol/L乙酸溶液恰好中和,所得溶液的pH等于7 |
| D.25℃时,pH=12的氨水和pH=2的H2SO4溶液等体积混合,所得溶液的pH大于7 |
将3.2 gCu投入到一定浓度的HNO3溶液中,恰好完全反应,产生NO2和NO的混合气体共 0.08 mol。则原溶液中HNO3的物质的量为
惰性电极电解一定浓度的硫酸铜溶液,通电一段时间后,向所得的溶液中加入0.2 mol Cu(OH)2后恰好恢复到电解前的浓度。则电解过程中转移的电子为
| A.0.4 mol | B.0.6 mol | C.0.2 mol | D.0.8 mol |
在水中加入等物质的量的Ag+、Pb2+、Na+、SO42-、 NO3-、Cl-,该溶液放在用惰性材料做电极的电解槽中,通电片刻,则氧化产物和还原产物的质量之比
| A.35.5:108 | B.16:207 | C.8:1 | D.108:35.5 |
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是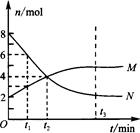
A.反应的化学方程式为:2M N N |
| B.t2时,正逆反应速率相等,达到平衡 |
| C.t3时,正反应速率大于逆反应速率 |
| D.t1时,N的浓度是M浓度的2倍 |
在一定温度下,可逆反应A(g)+3B(g)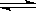 2C(g)不能表示达到平衡的标志的是
2C(g)不能表示达到平衡的标志的是
(1)C的生成速率与C的分解速率相等;(2)单位时间内amol A生成,同时生成3amol B;(3)A、B、C的浓度不再变化;(4)混合气体的总压强不再变化;(5)混合气体的物质的量不再变化;(6)单位时间消耗amol A,同时生成3amol B;(7)A 、B、C的分子数目比为1:3:2。
A.(2)(5) B.(1)(3) C.(2)(7) D.(5)(6)