(10分)下列各组物质的分离或提纯,应选用下述方法的哪一种?(用编号填空)
| A.分液 | B.过滤 | C.萃取 | D.蒸馏 |
E、蒸发结晶 F、加热分解
① 除去Ca(OH)2溶液中悬浮的CaCO3 ;
② 从碘水中提取碘 ;
③ 用自来水制取蒸馏水 ;
④ 除去碳酸钠固体中少量的碳酸氢钠固体 ;
⑤ 分离植物油和水 ;
在标准状况下,(a)4 g H2(b)11.2 L O2(c)27mL H2O中,所含分子数最多的是(填序号)①_________,含原子数最多的是②,体积最大的是③,质量由大到小的顺序是④。
根据图示填空。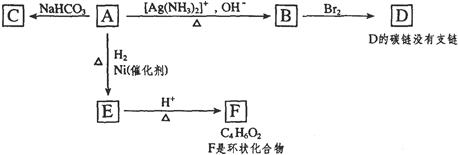
(1)化合物A含有的官能团是。
(2)1mol A与2mo H2反应生成1moE,其反应方程式是。
(3)与A具有相同官能团的A的同分异构体的结构简式是。
(4)B在酸性条件下与Br2反应得到D,D的结构简式是。
(5)F的结构简式是。由E生成F的反应类型是。
(8分)将等物质的量的A、B混合于2L的密闭容器中,发生如下反应:
3A(g)+B(g) xC(g)+2D(g),经5min后,测得D的浓度为0.5mol·L-1,C的平均反应速率是0.1mol/(L。min),且此时A、B的物质的量浓度之比为3∶5。求:
xC(g)+2D(g),经5min后,测得D的浓度为0.5mol·L-1,C的平均反应速率是0.1mol/(L。min),且此时A、B的物质的量浓度之比为3∶5。求:
(1)此时A的浓度为 .反应开始前放入容器中A、B的物质的量
(2)B的平均反应速率 .
(3)x的值是多少 .
(4)下列叙述能证明该反应已达到化学平衡状态的是。
A.溶器内压强不再发生变化
B.A的体积分数不再发生变化
C.容器内气体分子总数不再发生变化
D.相同时间内消耗3nmolA的同时消耗nmolB
E. 混合气体的平均相对分子质量不再变化
(8分)有A、B、C、D四种短周期元素,其原子序数依次增大。A、B可形成A2B和A2B2两种化合物,B、C同主族且可形成CB2和CB3两种化合物。回答下列问题。
(1)A2B2的电子式为____________。
(2)CB2通入A2B2溶液中可被氧化为W,用W的溶液(体积为1 L,假设变化前后溶液体积变化忽略不计)组装成原电池(如图所示)。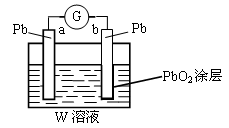
在b电极上发生的反应可表示为:PbO2+4H++SO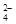 +2e-=PbSO4+2H2O,则在a电极上发生的反应可表示为_________________。若电池工作一段时间后,a极消耗0.05 mol Pb,则W的浓度由质量分数39 % (密度1.3 g / cm3)变为______mol /L。
+2e-=PbSO4+2H2O,则在a电极上发生的反应可表示为_________________。若电池工作一段时间后,a极消耗0.05 mol Pb,则W的浓度由质量分数39 % (密度1.3 g / cm3)变为______mol /L。
(3)金属元素E是中学化学常见元素,位于元素周期表的第四周期。该元素可与D形成ED2和ED3两种化合物。将E的单质浸入ED3溶液中(如下图甲所示),溶液由黄色逐渐变为浅绿色,该反应的离子方程式为____________________________________。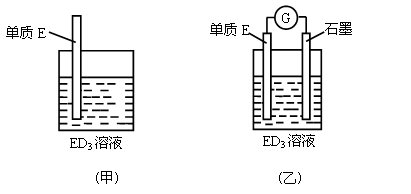
(4)依据(3)中的反应,可用单质E和石墨为电极设计一个原电池(图乙),则在该原电池工作时,石墨一极发生的反应可以表示为______________________________。
下列变化①碘的升华②烧碱熔化③氯化钠溶于水④氯化氢溶于水⑤氧气溶于水⑥氯化铵受热分解。其中(1)未发生化学键破坏的是;(2)仅发生离子键破坏的是_____;(3)仅发生共价键破坏的是(不包括范德华力);(4)既发生离子键又发生共价键破坏的是_____。