用铂电极电解CuCl2与CuSO4的混合溶液(浓度均为2 mol/L)50 mL,当阴极析出9.6 g固体时,标准状况下阳极得到的气体的体积是
| A.3.36 L | B.2.8 L | C.6.72 L | D.4.48 L |
已知温度T时水的离子积常数为KW,该温度下,将浓度为a mol·L-1的一元酸HA溶液与b mol·L-1的一元碱BOH溶液等体积混合,可判定该溶液呈中性的依据是
| A.a=b |
| B.混合溶液的pH=7 |
| C.混合溶液中,c(H+)= mol·L-1 |
| D.混合溶液中,c(H+)+c(B+)=c(OH-)+c(A-) |
25 ℃时,水的电离达到平衡:H2O  H++OH-,下列叙述正确的是
H++OH-,下列叙述正确的是
| A.向水中加入稀氨水,平衡逆向移动,c(OH-)降低 |
| B.向水中加入少量固体硫酸氢钠,c(H+)增大,Kw增大 |
| C.降温,使平衡左移,c(H+)减小,溶液呈碱性 |
| D.将水加热,Kw增大,pH减小 |
对于xA(g)+yB(g)  zC(g)+wD(g)的平衡体系,当升高温度时,体系的平均相对分子质量从26变为29,则下列说法中正确的是
zC(g)+wD(g)的平衡体系,当升高温度时,体系的平均相对分子质量从26变为29,则下列说法中正确的是
| A.x+y>z+w, 正反应是放热反应 | B.x+y>z+w,正反应是吸热反应 |
| C.x+y<z+w,逆反应是放热反应 | D.x+y<z+w,正反应是吸热反应 |
下列各离子方程式中,属于水解反应的是
A.HCO3-+H2O  H3O++CO32- H3O++CO32- |
B.NH4++H2O  NH3·H2O+OH- NH3·H2O+OH- |
C.PO43-+H2O  HPO42-+OH- HPO42-+OH- |
D.H2O+H2O  H3O++OH- H3O++OH- |
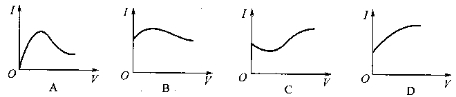
向0.1 mol·L-1醋酸溶液中逐滴加入氨水至过量时,溶液的导电能力将发生相应的变化,其电流强度(I)随加入氨水的体积(V)变化的曲线关系是下图中的