用来测定空气成分的方法很多,如图所示的是小明用红磷在空气中燃烧的测定方法。实验过程是: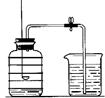
第一步:将集气瓶容积划分为五等份,并做好标记。
第二步:点燃燃烧匙内的红磷,伸入集气瓶中并把塞子塞紧。
第三步:待红磷熄灭并冷却后,打开弹簧夹,发现水被吸入集气瓶中,进入集气瓶中水的体积约为集气瓶总容积的1/5。请回答下列问题:
(1)上面的实验同时证明了氮气有 的化学性质。
(2)实验完毕,若进入集气瓶中水的体积不到总容积的1/5,你认为导致这一结果的原因可能是 。
(3)第二步中发生反应的文字表达式为________________________________。
(4)某同学对实验进行反思后,提出了改进方法(如图所示 ),你认为改进后的优点是: 。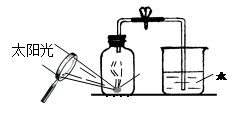

为了探究某脱氧剂的成分(由铁和某种单质组成)及利用该脱氧剂测定空气中氧气含量,兴趣小组进行了如下实验:
(1)探究脱氧剂成分
【实验观察】脱氧剂为灰黑色粉末,若在空气中放置一段时间,有红棕色固体生成,这是由于铁与空气中的 和 反应生成了铁锈。
【实验探究】新取一定量的脱氧剂,将铁分离。取剩余固体在空气中充分灼烧,收集产生的气体,并将该气体通入澄清石灰水,发现澄清石灰水变浑浊。
【实验结论】该脱氧剂中还含有 (填化学式)。写出澄清石灰水变浑浊的化学式表达式: 。
(2)测定空气中氧气含量(如图1):
步骤1:在注射器中放入足量脱氧剂粉末(体积为2mL),封闭。
步骤2:打开弹簧夹,将活塞向右拉至一定距离,关闭弹簧夹。
步骤3:不断轻轻晃动注射器,至活塞位置不再发生变化。
【数据处理】:计算得出氧气约占空气体积的1/5。
【实验对比】:实验室常通过燃烧红磷法测定空气中氧气的含量(装置如图2),用燃烧红磷法多次实验发现,集气瓶内上升的水面始终小于瓶内原有空气体积的1/5。
【拓展研究】查阅资料得知,当空气中氧气的体积分数降至约为7%以下时,红磷不再燃烧,所以用该法测定结果不够准确。请写出红磷燃烧的化学式表达式 。
与燃烧红磷法相比,脱氧剂法测定空气中氧气含量除了环保外,还具有的优点是 。
小明发现一种淡黄色的粉末可以用于杀菌、消毒和漂白。
【定性探究】探究该固体的成分。
【提出问题】该淡黄色固体的化学成分是什么?
【查阅资料】(1)硫单质是一种淡黄色固体,难溶于水,在空气中点燃硫单质,生成一种无色、有刺激性气味的气体。
(2)过氧化钠(Na2O2)是一种淡黄色固体,能与水反应,生成气体并放出大量的热。
【设计实验方案】
方案一:取少量该固体粉末于试管中,加2mL水,振荡并观察现象。
方案二:在燃烧匙里放少量该固体,在酒精灯上加热,观察现象。
比较以上两方案,你认为的最佳方案是 ,理由是(从环保或操作角度分析) 。
【实验验证并得出结论】小明向盛有少量该固体的试管中加入2mL水,立刻观察到有无色气泡产生,并且验证出该反应同时生成了氢氧化钠(NaOH)。通过实验验证,确定该淡黄色粉末为过氧化钠。
小明想对生成的气体成分判断,他提出了以下两种假设:①该气体是CO ②该气体是O2你认为上述假设哪个更合理 (填“①”或“②”)。理由是是 。
请设计一个实验,验证合理假设(写出简要操作步骤、实验现象和结论)。(共2分)
| 操作步骤 |
实验现象 |
结论 |
【分析】 过氧化钠与水反应的符号表达式为 。
【定量探究】 78克过氧化钠与多少克二氧化碳中所含氧元素的质量相等?
(列式计算)
我国劳动人民早在五千年前就会使用木炭炼铜.在化学实验室里模拟炼铜,既可用传统的实验装置(见图甲),又能用改进的微型实验装置(见图乙).化学兴趣小组采用图乙装置,开展以下探究活动.
【提出问题】木炭与CuO反应所得红色固体中含有什么物质?
【查阅资料】
(1)木炭与CuO的反应是:C+2CuO 2Cu+CO2↑,若该反应进行的不彻底,产物中还有氧化亚铜(Cu2O).
2Cu+CO2↑,若该反应进行的不彻底,产物中还有氧化亚铜(Cu2O).
(2)Cu2O是红色固体,能与稀硫酸反应得到铜和硫酸铜溶液:Cu2O+H2SO4====Cu+CuSO4+H2O
【作出猜想】红色固体的成分:①全部是Cu;②全部是Cu2O;③ .
【实验探究】
(1)取木炭、CuO两种黑色粉末适量,再也少许CaC12(能降低反应温度,加快反应速率)均匀混合,然后将黑色粉末装入长柄V形玻璃管的直管内.
(2)按图乙连好实验装置,然后加热反应物;2分钟后,黑色粉末出现红热现象,同时澄清的石灰水 ,写出该反应的化学方程式______________________
(3)待玻璃管冷却后,提取里面的红色固体,进行如下的验证:
| 步骤 |
现象 |
结论 |
| Ⅰ.取1.44g红色固体装入试管,滴入足量 的 ,充分反应 |
红色固体部分减少,溶液变 为 色 |
猜想 错误 |
| Ⅱ.滤出试管中残留的红色固体,洗涤干燥 称其质量为1.04g |
猜想 正确 |
【评价反思】
(1)使用图乙装置与使用图甲装置相比,其优点是 (写出1条即可).
(2)若要证明CaC12是该反应的催化剂,还需要验证CaCl2的 .
工业铁红的主要成分是Fe2O3,还含有少量的FeO、Fe3O4。为了测定铁红中铁元素的质量分数,兴趣小组的同学进行了如下实验,请你参与过程分析。
[资料1]碱石灰既能吸收水又能吸收二氧化碳;浓硫酸可以吸收水蒸气;
[资料2]实验室常用氢氧化钠溶液来除去CO2反应生成碳酸钠和水;用澄清的石灰水
来检验CO2气体;
[资料3]草酸晶体(H2C2O4·3H2O)在浓H2SO4作用下受热分解,化学方程式为:
H2C2O4·3H2O CO2↑+ CO↑+ 4H2O
CO2↑+ CO↑+ 4H2O
(1)下列可用作草酸分解制取气体的装置是 (填字母编号)。
【问题讨论】用下图所示装置进行实验:
A B C D E F
(2)实验前应先 。
(3)进入D中的气体是纯净、干燥的CO,则A、C中的试剂依次是 、 (填字母编号)。
a.浓硫酸 b.澄清的石灰水 c.氢氧化钠溶液
(4)写出A装置中发生的化学反应方程式 。
(5)B装置的作用是 。
(6)对D装置加热前和停止加热后,都要通入过量的CO,其作用分别是:
①加热前 。 ②停止加热后 。
(7)写出D装置中所发生反应的一个化学方程式 。
【数据分析与计算】
[资料4]铁的常见氧化物中铁的质量分数:
| 铁的氧化物 |
FeO |
Fe2O3 |
Fe3O4 |
| 铁的质量分数 |
77.8% |
70.0% |
72.4% |
(8)称取铁红样品10.0 g,用上述装置进行实验,测定铁红中铁的质量分数。
①D中充分反应后得到Fe粉的质量为m g,则 < m < 。
② 实验前后称得E装置增重6.6g,则此铁红中铁的质量分数是 。
【实验评价】
反思1:本实验中如果缺少C装置(不考虑其它因素),则测得样品中铁的质量分数会 (填“偏小”、“不变”或“偏大”)。
反思2:请指出【问题讨论】中实验装置的一个明显缺陷 。
小明参观某养鱼池时,好奇地发现农民向养鱼池撒一种叫做过氧化钙的淡黄色
固体,用来增加鱼池中的含氧量。小明刚学完氧气的实验室制法,于是他想可否用过氧化钙制取氧气。
【提出问题】过氧化钙可否用于制取氧气?
【查阅材料】部分内容如下:过氧化钙(CaO2)室温下稳定,在300℃时分解生成氧气,可做增氧剂、杀菌剂等。
【猜想与验证】
小明依据上述材料,提出猜想Ⅰ: ,然后进行以下实验:
| 实验装置 |
实验主要过程 |
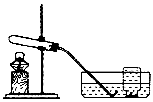 |
检验装置气密性。 加入过氧化钙于试管中,加热,导管口有大量气泡冒出。 收集满一瓶气体。 ④ 停止加热。熄灭酒精灯前,应___________________。 ⑤ 检验气体。方法是______________________。 |
(2)小明联想到农民用过氧化钙增加鱼池中的含氧量,提出猜想Ⅱ。
猜想Ⅱ:过氧化钙与水反应可制取氧气
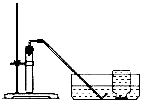 |
检验装置气密性。 ② 加入过氧化钙和水后,有少量细小气泡缓慢放出,在导管口几 乎收集不到气体。该装置放置到第二天,集气瓶只收集到极少量 气体,振荡试管后仍有少量细小气泡缓慢放出。 |
【实验结论】不能用过氧化钙与水反应制取氧气。
【分析与反思】
①虽然没有快速收集到大量氧气,但由此实验现象,小明认为农民用过氧化钙做增氧剂的主要原因是________________________。
②小明希望对此实验进行改进,使该反应加快,你能帮他提出建议吗?你的合理建议:
_________________________。
以上建议是否可行,还需进一步通过实验验证。