下列两列文字中,左面是处理天然水的几个步骤,右面是这些步骤起的作用,请用线把它们连接起来。
沉降 灭菌
加入明矾 除去颗粒较大的不溶性杂质
过滤 除去颗粒较小的不溶性杂质
通入氯气 吸附悬浮杂质而沉降
根据元素的原子结构和性质,科学家将元素有序地排列起来,得到元素周期表。
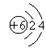
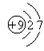
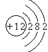
(1)以下是部分元素的原子结构示意图:
| H |
Li |
C |
F |
Na |
Mg |
Cl |
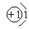 |
 |
 |
 |
 |
 |
 |
中的“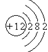 ”表示 ,它形成的离子与Cl-形成的化合物中氯元素的化合价为。
”表示 ,它形成的离子与Cl-形成的化合物中氯元素的化合价为。
(2)下面是元素周期表的一部分(1、2、3周期),从原子结构示意图和周期表可知:
主族(纵列)序数等于原子最外层电子数,周期(横行)序数=。
(3)请用元素符号将碳元素填在周期表的相应位置。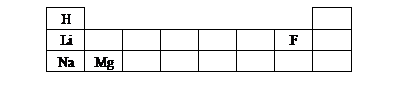
(4)原子的结构决定元素的性质。F元素的化学性质与 相似。
某兴趣小组利用下列装置进行实验室制取和收集气体的实验,请回答: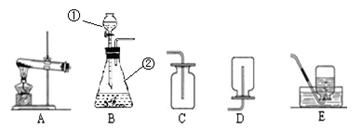

(1))在上图中写出标数字的仪器名称:①__________②________
(2)若用加热高锰酸钾来制取并收集较干燥的氧气,应选用的制取和收集装置是(填装置序号),反应的表达式为 ,若用E装置收集氧气,水槽中出现紫红色,最可能的原因是;实验结束时,应该先,后,目的为了。若用E装置收集O2,应在
时开始收集;若用C装置收集O2,验满的方法是。
(3)用双氧水和二氧化锰制取氧气时,应该选用的发生装置是(填装置序号),反应文字表达式为___________________。若反应很剧烈,据此提出实验安全注意事项是_________(填序号)①控制液体的滴加速度②用体积较小的反应容器③加热反应物
(4)实验室制取二氧化碳,选用的药品是_____和(填名称),反应的表达式是_________。若用C装置收集CO2,验满的方法是。为了得到二氧化碳气体,甲、乙两个化学兴趣小组分别设计了如上图所示的F发生装置。你认为可行吗?,若不合理,应如何改正?。
(5)加热铜绿应选择装置进行实验(填装置序号),反应表达式为。若实验结束发现试管破裂的原因可能是(写出一种可能的原因)。
(6)联想:氨气(NH3)是一种密度比空气小,极易溶于水的气体,实验室可用加热氯化铵和氢氧化钙固体混合物制得氨气。氨气在加热条件下能与氧化铜反应生成铜、水和空气中含量最多的气体。制取氨气应选择装置(填装置序号)。请写出氨气和氧化铜(CuO)反应的表达式。
写下列反应的表达式,并回答问题
(1)镁条燃烧 ,利用镁条燃烧能的现象,镁被用来制造烟花;
(2)加热碳酸氢铵,该反应基本类型为。
(3)硫在氧气中燃烧,现象。
(4)铁丝在氧气中燃烧 ,实验前要在瓶内,目的是防止,使集气瓶炸裂;该反应基本类型为。
(5)二氧化碳通入澄清石灰水,此反应可用于检验。
)水是生命之源,生活中净化水的方法很多。
下图是某同学制作的简易净水器: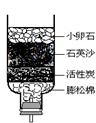
在农村人们常常饮用河水,河水中常含有大量的泥沙、悬浮物和细菌等杂质,一般可用次氯酸杀死细菌。将漂白粉(主要成分是次氯酸钙)溶于水可生成氯化钙和次氯酸。下列是某户居民在饮用水之前对河水的处理步骤:
河水→A(加入明矾)→B(沉淀)→C(过滤)→D(加入漂白粉)→净水
(1)可以除去较大颗粒、悬浮物杂质的步骤是;
(2)能够消毒、杀菌的步骤是;
(3)如用右图装置净化水,活性炭的作用是。
(4)该农户得到的净化水是混合物 ,原因是;
净化后是硬水还是软水?我认为可用来检验。长期饮用硬水对人体不利,要降低水的硬度,生活中通常采用的方法。
(5)下图是某同学用来除去水中难溶性杂质时所采用的过滤装置图。试回答: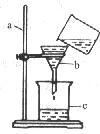
写出标号仪器的名称:a,b__,C__________。
该图中存在明显三处的错误是:
①;
②;
③
(6)在过滤时,若经过两次过滤后滤液仍然浑浊,其原因可能是_;(要求写出两个方面的原因)。
实验是化学学习的一种重要手段,如利用电解水实验可探究水的组成。请根据电解水实验回答下列问题:
(1)通电后电极上出现,并汇集到试管上端。负极产生的气体是。检验正极产生的气体的方法是_______________.
(2)实验时常在水中加入硫酸或氢氧化钠,目的是______________。
(3)水通电过程中发生变化的微粒符号是_____________文字表达式为____。该变化属于______________________反应(填基本类型)
(4)在某次电解水的实验中加入了少量的NaOH溶液,测得了分别与电源正负两极相连的阳、阴两极上产生的气体的实验数据如下:
仔细分析以上实验数据,1~6分钟内阴、阳两极生成的气体体积之比大于2:l,可能的原因是氧气比氢气__________溶于水(填“易”或“难”)