下面关于Na2CO3和NaHCO3性质的叙述,正确的是( )
| A.受热时NaHCO3比Na2CO3稳定 |
| B.在水中NaHCO3比Na2CO3溶解性大 |
| C.质量相等的Na2CO3和NaHCO3分别与足量盐酸反应,NaHCO3放出的CO2比Na2CO3多 |
| D.物质的量相等的Na2CO3和NaHCO3分别与足量盐酸反应,放出的CO2的物质的量之比为2︰1 |
某有机物的结构简式如下,它可能发生的反应类型有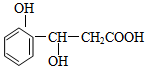
①取代②加成③消去④水解⑤酯化⑥中和⑦氧化⑧加聚
| A.①②③⑥ | B.②③④⑤⑧ | C.①②③⑤⑥⑦ | D.③④⑤⑥⑦ |
既可以发生消去反应,又能被氧化成醛的物质是
| A.2—甲基—1—丁醇 | B.2,2—二甲基—1—丁醇 |
| C.2—甲基—2—丁醇 | D.2,3—二甲基—2—丁醇 |
下列化合物中,既能发生消去反应生成烯烃,又能发生水解反应的是()
关于乙醇在不同的反应中断裂化学键的说法错误的是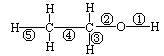
| A.与金属钠反应时,键①断裂 |
| B.在Cu催化下与O2反应时,键①、③断裂 |
| C.与乙酸在浓硫酸作用下反应时,键②断裂 |
| D.与浓硫酸共热至140℃时,键①或键②断裂;共热至170℃时,键②、⑤断裂 |
由2-氯丙烷制取少量的1,2-丙二醇时,需要经过下列哪几步反应
| A.加成→消去→取代 | B.消去→加成→水解 |
| C.取代→消去→加成 | D.消去→加成→消去 |