下列图示与对应的叙述相符的是( ) 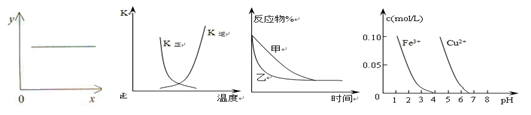
图1 图2 图3 图4
A.图1表示反应2NO(g)+2CO(g)  N2(g)+2CO2(g)平衡常数K 随NO物质的量的变化 N2(g)+2CO2(g)平衡常数K 随NO物质的量的变化 |
B.图2中表示反应2A(g) + B(g) 2C(g) ΔH > 0的平衡常数K随温度的变化 2C(g) ΔH > 0的平衡常数K随温度的变化 |
C.图3表示压强对可逆反应2A(g)+2B(g) 3C(g)+D(s)的影响,乙的压强比甲的大 3C(g)+D(s)的影响,乙的压强比甲的大 |
| D.据图4,若除去CuSO4溶液中的Fe3+可向溶液中加入适量CuO至pH在5左右 |
下列反应试剂和条件能增大有机化合物不饱和度的是
| A.氢氧化钠的醇溶液,加热 | B.氢氧化钠的水溶液,加热 |
| C.稀硫酸,加热 | D.银氨溶液 |
通常情况下,用到的下列反应试剂所发生的反应,能使反应物碳链缩短的是
| A.氢氧化钠的水溶液 | B.氢氧化铜碱性悬浊液 |
| C.溴的四氯化碳溶液 | D.氢气(镍作催化剂) |
下列说法正确的是
| A.酸性高锰酸钾溶液有强氧化性,苯和苯的同系物均能被它氧化 |
| B.氯化铁溶液和苯酚溶液反应非常灵敏,可用此反应做苯酚的鉴别和定量测定 |
| C.乙烯和苯都可以使溴水褪色,两者的褪色原理是相同的 |
| D.银氨溶液有一定的氧化性,在一定条件下可以将醛基氧化为羧基 |
把7.4 g Na2CO3·10H2O 和 NaHCO3组成的混合物溶于水配成100mL溶液,其中c(Na+)=0.6mol/L。若把等质量的混合物加热至恒重,残留物的质量是
| A.3.18g | B.2.12g | C.4.22g | D.5.28g |
新型净水剂—高铁酸钾(K2FeO4)为暗紫色固体,可溶于水。工业上制备K2FeO4的常用方法之一是次氯酸盐氧化法:①2FeCl3+10NaOH+3NaClO=2Na2FeO4+9NaCl+5H2O、②Na2FeO4+2KOH=K2FeO4+2NaOH。下列说法不正确的是
| A.反应①为氧化还原反应,反应②为复分解反应 |
| B.反应①中氧化产物与还原产物物质的量之比为2:9 |
| C.反应②的产物K2FeO4中Fe为+6价,具有强氧化性,能杀菌消毒 |
| D.若有2mol FeCl3发生反应,转移电子的物质的量为6 mol |