将足量的大理石加入到100g溶质质量分数为14.6%的稀盐酸中,充分反应后可得多少克二氧化碳。
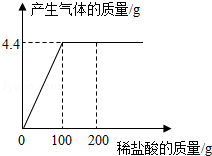
取CaCl2和CaCO3的混合物12.5g于烧杯中,向其中滴加一定溶质质量分数的稀盐酸,请加稀盐酸的质量与产生气体质量的关系如图所示。求:
(1)混合物CaCO3中的质量为 ;
(2)稀盐酸中的溶质质量分数为 ;
(3)恰好完全反应时,所得不饱和溶液中溶质的质量分数?(写出计算过程,计算结果精确到0.1%)
(5分)铁的氧化物有三种,分别是FeO、Fe2O3和Fe3O4.某固体粉末可能含有一种或两种铁的氧化物.取23.2克固体粉末,向其中通入足量一氧化碳并加热(假设固体完全反应),将反应生成的气体通入足量的澄清石灰水中,生成40.0克沉淀.试计算:
(1)反应生成二氧化碳的质量为多少克?(要求写出计算过程)
(2)固体粉末中含有的铁的氧化物可能为 或 .
铜锌合金又称假黄金。向盛有30g铜锌合金粉末样品的烧杯中逐渐加入稀硫酸,生成氢气的质量与加入稀硫酸的质量关系如图所示,计算:
(1)充分反应后生成氢气的质量为 g。
(2)合金样品中锌的质量。
(3)恰好完全反应时,所得溶液溶质的质量分数。(结果保留一位小数)

柠檬酸铁铵(化学式为C 6H 8FeNO 7)添加到食盐中可作营养增长剂,且能使食盐保持干燥。某品牌食盐配料表上注有:柠檬酸铁铵≤25mg/kg。
(1)柠檬酸铁铵中碳、氧元素的质量比为 ;
(2)1kg这种食盐中含铁元素的质量最多为 mg (结果保留一位小数 )。