(7分) 在足量的稀氯化亚铁溶液中加入1~2滴液溴,振荡后溶液变为黄色。
(1)甲同学认为是Br2溶于水变成黄色溶液;乙认为是Fe2+被氧化成Fe3+使溶液变成黄色。
(2)现提供试剂:
| A.酸性高锰酸钾溶液 | B.氢氧化钠溶液 |
| C.四氯化碳 | D.硫氰化钾溶液 |
请判断 (填“甲”或“乙”)的推断正确,并用两种方法加以验证,写出选用的试剂编号及实验中观察到的现象:
| |
选用试剂 |
实验现象 |
| 第一种方法 |
|
|
| 第二种方法 |
|
|
(3)若选用淀粉碘化钾溶液判断哪位同学推断正确,是否可行?(填“可行”或“不可行”): ;理由: 。
某学生设计了如下的实验装置图用于制备干燥纯净的氯气。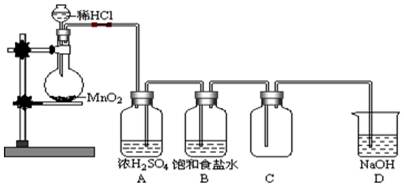
(1)指出上 述装置图中的错误(有几处答几处)
述装置图中的错误(有几处答几处)
①铁架台上少酒精灯____________________②________________________________
③____________________________________ ④________________________________
⑤____________________________________ ⑥_________________________________
(2)改正后的装置图中,洗气瓶中的饱和食盐水、浓硫酸以及氢氧化钠溶液各起什么作用?
①饱和食盐水的作用_________________;②浓硫酸的作用____________________;
③氢氧化钠溶液的作用_______________________________。
(3)写出烧瓶中发生反应的化学方程式并注明反应条件:_____________________________
实验室需要0.1 mol/L NaOH溶液450 mL。根据这种 溶液的配制情况回答下列问题:
溶液的配制情况回答下列问题:
(1)如图所示的仪器中配制溶液肯定不需要的是 (填序号),本实验所需玻璃仪器E规格为 mL。
(2)下列有关容量瓶的说法中,不正确的有 (填序号)。
| A.能配制一定体积准确浓度的标准溶液 | B.可长期贮存溶液 |
| C.能用来加热溶解固体溶质 | D.使用前必须检查是否漏水 |
(3)在配制NaOH溶液实验中,其他操作均正确。若定容时仰视刻度线,则所配制溶液浓度
0.1 mol/L(填“大于”“等于”或“小于”)。
(8分)根据下图提供的仪器装置,完成提纯并测定Na2CO3样品纯度(其中只含NaHCO3杂质)的实验。
| 序号 |
① |
② |
③ |
④ |
⑤ |
⑥ |
⑦ |
| 仪 器 及 装 置 |
 |
 |
 |
 |
 |
 |
 |
请回答下列问题:
实验一:测定Na2 CO3样品中的NaHCO3分解放出的二氧化碳的体积。
CO3样品中的NaHCO3分解放出的二氧化碳的体积。
(1)连接装置的正确顺序是:_________接_________接_________接_________。(写序号)
(2)完成实验一尚缺的仪器是:___________________________。
(3)气体应从装置⑤的_________端进入。(写字母)
实验二:测定经实验一后的固体物质与盐酸反应放出二氧化碳的体积。
(4) 连接装置的正确顺序是:_________接_________接_________接_______(写序号)
(5)当实验一测得产生的二氧化碳为a mol,当实验二测得产生的二氧化碳为b mol。则该样品中碳酸钠纯度的实验值为:______________________。与理论值比较,实验结果_______(填:偏大、偏小或相等);若要使实测值更接近于理论值,该实验应怎样改进?_____(用文字简要说明)
(6分)(1)用18.0 mol/L H2SO4配制100 mL 1.00mol/L H2SO4,则需要的实验仪器除了烧杯、玻璃棒、胶头滴管以外还应该有:______
配制过程中,下列情况会使配制结果偏高的是(填序号)____
①定容是俯视刻度线观察液面
②容量瓶使用时未干燥
③定容后经振荡、摇匀、静置,发现液面低于刻度线,再加蒸馏水补至刻度
④容量瓶盛过H2SO4溶液,使用前未洗涤
(2)在容量瓶使用方法中,下列操作不正确的是(填字母)_________
A.使用容量瓶前检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配液润洗
C .配制溶液时,如果试样是液体,用量筒量取试样后直接倒入容量瓶中,缓慢加入蒸馏水到接近标线1~2㎝处,再改用胶头滴管加蒸馏水到刻度线
.配制溶液时,如果试样是液体,用量筒量取试样后直接倒入容量瓶中,缓慢加入蒸馏水到接近标线1~2㎝处,再改用胶头滴管加蒸馏水到刻度线
D.盖好瓶塞,用食指顶住瓶塞,用另一只手托住瓶底,把容量瓶倒转摇匀
用A、B、C三种装置都可制取溴苯。请仔细分析三套装置,然后回答下列问题:
(1)写出三个装置中都发生反应的化学方程式:、 ;写出B的试管中还发生的反应化学方程式;
;写出B的试管中还发生的反应化学方程式;
(2)装置A、C中长导管的作用是;
(3)B、C装置已连接好,并进行了气密性检验,也装入了合适的药品,接下来要使反
应开始,对B应进行的操作是,对C应进行的操
作是;
(4)A中存在 加装药品和及时密封的矛盾,因而在实验中
加装药品和及时密封的矛盾,因而在实验中 易造成的不良后果是
易造成的不良后果是
。