过氧化氢溶液在二氧化锰作催化剂的条件下能迅速分解成氧气和水。分液漏斗可以通过调节活塞控制液体滴加速度。回答下列问题:
⑴分液漏斗中应放入的物质是 ,锥形瓶中应放入的物质是 。
⑵要收集一瓶纯净的氧气应选择上图中的装置 (填字母)
⑶某同学在观察到锥形瓶内有大量气泡时,开始用C装置收集氧气,过一断时间后用带火星的木条伸入瓶口、瓶中、瓶底,都未见木条复燃。其原因是 。
⑷若实验时用此法代替高锰酸钾加热制氧气,优点是 (填序号)
A.生成物中只有氧气 B.不需加热 C.需加热
⑸装置A中反应剧烈,据此提出实验安全注意事项是( )
A.控制液体的滴加速度 B.用体积小的锥形瓶 C.加热反应物
(7分)某化学实验室产生的废液中含有Fe3+、Cu2+、Ca2+、Cl-四种离子,为了处理废液,回收金属并制备氯化铁晶体,现设计如下实验过程(部分):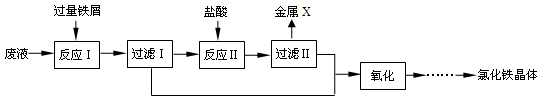
(1)金属X的化学式为。实验室进行过滤操作除需要用到烧杯、玻璃棒和铁架台(带铁圈)外,还需要的实验用品是。
(2)已知“反应Ⅰ”中,2FeCl3+ Fe=3FeCl2,发生的另一反应化学方程式为;
“反应Ⅱ”的化学方程式为。
(3)“氧化”中,化合价发生变化的金属元素是。
红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”,其标签如下图所示。同学们对一包久置的“504双吸剂”固体样品很好奇,设计实验进行探究。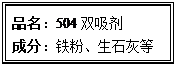
【提出问题】久置固体的成分是什么?
【查阅资料】铁与氯化铁溶液在常温下发生反应生成氯化亚铁。
【作出猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3。
久置固体中可能含有Ca(OH)2的原因是(用化学方程式表示)。
【实验探究1】
甲同学的方案:
| 实验操作 |
实验现象 |
实验结论 |
| ⑴取少量固体放于试管中,加足量蒸馏水溶解,静置后取上层清液滴加无色酚酞溶液。 |
固体溶解时试管外壁发烫,试管底部有不溶物,溶液变红。 |
固体中一定含有① 和氢氧化钙。 |
| ⑵另取少量固体放于试管中,滴加足量稀盐酸。 |
固体逐渐消失,有大量无色气体产生,得到浅绿色溶液。 |
固体中一定含有②, 一定不含Fe2O3。 |
| ⑶将步骤⑵中产生的气体通入到澄清的石灰水中。 |
③ |
固体中一定含有CaCO3。 |
【实验质疑】
⑴乙同学认为甲同学的实验中并不能得出一定含Ca(OH)2的结论,理由是
。
⑵丙同学认为甲同学的实验并不能得出一定不含Fe2O3的结论,理由是(用化学方程式表示)、。
【实验探究2】
乙、丙同学设计如下实验方案继续验证: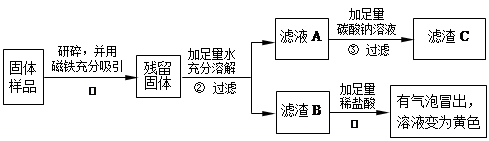
⑴ 乙、丙同学实验中又能得出固体样品中一定还含有。
⑵ 乙同学经过实验测得上述滤渣C(CaCO3 )的质量为1.0 g,计算滤液A中含氢氧
化钙的质量。(写出解题过程)
⑶ 丙同学经过实验测得上述残留固体中含钙物质的总质量为1.6 g,滤渣B中CaCO3的质量为1.0 g。
【实验结论】综合上述实验以及乙、丙两位同学的实验数据,久置固体的成分是:
(6分)某活动小组的同学正在探究酸碱溶液恰好完全反应的实验。
【设计与评价】
小香的方案:向盛稀盐酸的试管中滴加两滴酚酞溶液,再逐滴滴加氢氧化钠溶液,边滴边振荡至恰好变为红色;
小坊的方案:向盛氢氧化钠溶液的试管中滴加两滴酚酞溶液,再逐滴滴加稀硫酸,边滴边振荡至恰好变为无色;
小香的方案中发生反应的化学方程式为(1) ______________________________________;
【实验过程】
实验时小香按照方案进行了正确的操作,小坊忘了加指示剂,一直没有观察到溶液变化。实验结束后两位同学把试管中的废液倒入同一废液缸中,溶液呈无色。这时有人提议“继续探究废液缸中溶质(除酚酞外)的成分”:
【猜想与判断】
小香认为:可能是NaCl、Na2S04 H2S04
小坊认为:可能是NaCl、Na2S04,、NaOH
大家一致认为,经理论分析可以判断:小坊的猜想一定(2) ___________ (填“正确”或“错误”),无需探究;
【交流与表达】小香为了证明自己的猜想,实验如下:取样,加入氯化钡溶液,观察到溶液中有白色沉淀产生,则猜想正确。小香的实验________ (填“能”或“不能”)得出结论,理由是(4) __________________________________________________________________;
【补充与完善】为了证明小香的猜想,我设计的实验是:取样,加入(5) ___________ (一种有色溶液),观察到的实验现象是(6) ______________________,证明该猜想正确。
某课外小组的同学以“氢氧化钠试剂瓶口白色粉末的成分”为课题,进行科学探究活动,请你也参与到他们的实验探究中。
【提出问题】氢氧化钠试剂瓶口的白色粉末的成分是什么?
【猜想与假设】(1)甲同学猜想是:Na2CO3
乙同学猜想是:NaOH Na2CO3
丙同学猜想是:
【收集证据】(2)甲同学为证明自己的猜想:他取少量固体于试管中,加水溶解后,向其中滴加几滴氢氧化钡溶液,有白色沉淀产生,于是他自己的猜想是正确的。乙同学认为甲同学的结论不正确,其理由是
。
乙同学为证明自己的猜想:他取少量甲同学实验后的溶液,向其中滴加几滴酚酞溶液,观察到无色酚酞溶液变红的现象。得出自己的猜想是正确的。丙同学不同意乙同学的结论,原因是在甲的实验操作中引入,导致乙的实验不能验证自己的猜想。
(4)丙同学认为,要想证明NaOH是否存在,应该除去Na2CO3后才能继续证明,于是丙同学重新取白色粉末溶于水,加入一定量的稀盐酸直至不再产生气泡,然后再滴加酚酞溶液,发现酚酞溶液不变色,于是他认为甲的猜想正确。
请你写出丙同学滴加稀盐酸后所有可能发生反应的方程式;
【反思与评价】
(5)请你帮助丙同学改进实验设计,。并观察到了现象。得出了白色粉末的成分为NaOH Na2CO3的结论。
实验小组研究盐酸、氢氧化钠、氢氧化钙三种物质的化学性质,做了如图所示的实验。请你利用图中所给药品和他们一起进行研究。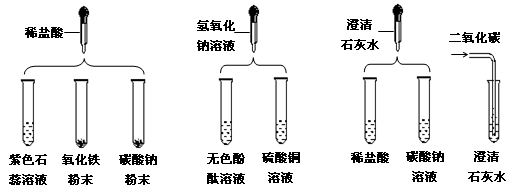
(1)实验后某试管中为黄色溶液,该试管中发生反应的化学方程式为。
(2)实验后某试管中为红色溶液,向其中加入足量的,溶液变为无色。由此推断,该试管中最初盛有的物质是。
(3)实验后某试管底部有蓝色絮状沉淀,继续向其中加入足量的,振荡后沉淀消失。
(4)实验后某试管的底部有白色固体,过滤后向滤液中滴加稀盐酸,开始时无明显现象,一段时间后有气泡出现。由此推断,该试管中最初发生反应的化学方程为。
(5)实验后某试管中只得到无色溶液,向其中加入足量的碳酸钠溶液,只产生气泡。那么该试管中最初发生反应的化学方程为。
(6)实验结束时,他们将实验废液倒入同一废液缸中,观察后,他们猜想最终的废液可能呈酸性。为了验证猜想,利用上述实验中未涉及到的酸的化学性质,另选药品进行实验:取少量废液样品于试管中,向其中加入一定量的,观察现象,证明最终的废液呈酸性。实验后为了避免废液造成不良后果 ,他们对废液进行了恰当处理。