下列关于热化学反应的描述中正确的是( )
A.500℃、30MPa下,将0.5mol N2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为:N2(g) + 3H2(g) 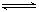 2NH3(g) △H=-38.6kJ·mol-1 2NH3(g) △H=-38.6kJ·mol-1 |
| B.HCl和NaOH反应的中和热ΔH=-57.3 kJ·mol-1,则H2SO4和Ca(OH)2反应的中和热ΔH=2×(-57.3)kJ·mol-1 |
| C.CO(g)的燃烧热是283.0 kJ·mol-1,则2CO2(g) =2CO(g)+O2(g)反应的ΔH=+2×283.0 kJ·mol-1 |
| D.1 mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热 |
下列叙述可用于说明H2+I2 2HI已达到平衡状态的是
2HI已达到平衡状态的是
| A.一个H-H键断裂的同时有一个I-I键组成 |
| B.一个H-H键断裂的同时有一个I-I键断裂 |
| C.一个H-I键形成的同时有一个H-H键断裂 |
| D.一个H-I键断裂的同时有一个H-H键形成 |
联氨(H2N-NH2)也叫肼,是重要的火箭燃料,它跟氨一样显碱性,能与酸反应生成盐。下列说法中不正确</PGN0049A.TXT/PGN>的是
A.肼是二元碱
B.肼具有还原性
C.从键能分析,肼的热稳定性比氨强
D.肼燃烧的产物是氮气和水
在密闭容器中,下列反应已达平衡:aA(气)+bB(气) cC(气)+dD(气)+Q如果升高温度或降低压强,则C(气)的物质的量都增大,试判断下列各组关系,哪组是正确的
cC(气)+dD(气)+Q如果升高温度或降低压强,则C(气)的物质的量都增大,试判断下列各组关系,哪组是正确的

下列反应的离子方程式正确的是
| A.氨气通入醋酸溶液中: CH3COOH+NH3=CH3COONH4 |
| B.澄清的石灰水跟盐酸反应: H++OH-=H2O |
| C.碳酸钡溶于醋酸: BaCO3+2H+=Ba2++H2O+CO2↑ |
| D.硝酸铁溶液中加入过量氨水: |

将0.2 mol/L NaF溶液与0.1mol/L稀硝酸等体积混合后,离子浓度的关系正确的是
