 下列叙述正确的是 ( )
下列叙述正确的是 ( )
| A.0.1 mol/L Na2CO3溶液中:c(Na+)>c(CO32->c(H+)>c(OH-) |
| B.pH=5的CH3COOH溶液和PH=5的NH4Cl溶液中,c(H+)前者大于后 |
| C.在Na2S溶液中加入AgCl固体,溶液中c(S2-)下降 |
| D.Na2CO3溶液加水稀释后,恢复至原温度,pH和Kw均减小 |
设NA为阿伏加德罗常数的值。下列说法正确的是
A.在反应5NH4NO3  2HNO3+4N2↑+9H2O中,每生成4 mol N2,转移电子数为10NA 2HNO3+4N2↑+9H2O中,每生成4 mol N2,转移电子数为10NA |
| B.12.5 mL 16 mol·L-1浓硫酸与足量铜反应,转移电子数为0.2NA |
| C.标准状况下,1.12L的SO3所含的原子数约为0.2NA |
| D.标准状况下,2.2gCO2气体中所含分子数为0.05NA |
下列的离子方程式中,书写正确的一项是
| A.氨水中通入过量CO2:2NH3·H2O +CO2= 2NH4++CO32-+H2O |
| B.稀硝酸中加入过量铁粉:3Fe + 8H++2 NO3-= 3Fe2++ 2NO↑ + 4H2O |
| C.钠与水反应Na+2H2O= Na+ +2OH-+H2 ↑ |
| D.Ca(ClO)2溶液中通入过量的二氧化硫气体:ClO-+SO2+H2O= HClO+HSO3- |
有关粒子在相应条件下能大量共存的是
| A.常温常压下混合气体:H2、F2、NO、O2 |
| B.能溶解Al2O3的溶液:NH4+、K+、Cl-、CO32- |
| C.c(H+)="1.0" mol·L-1的溶液中:K+、Fe3+、SO42-、I- |
| D.澄清透明的溶液中:Na+、K+、MnO4-、[Al(OH)4]- |
用下列有关实验装置进行相应实验,错误的是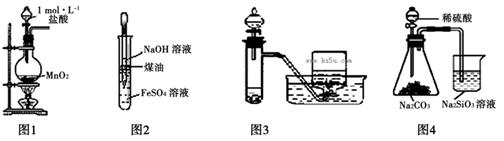
A.用图1所示装置实验室制取少量Cl2
B.用图2所示装置制取及观察Fe(OH)2
C.用图3所示装置用H2O2溶液制备O2
D.用图4所示装置比较S、C、Si的非金属性强弱
下列关于有机物的说法中错误的是
| A.乙烷和乙烯都能与氢气在一定条件下发生加成反应 |
| B.苯和乙烯都能使溴水褪色,但其原理是不同的 |
| C.甲烷和乙醇均能发生取代反应 |
| D.乙醇、乙酸和乙酸乙酯能用饱和Na2CO3溶液鉴别 |