某待测液中可能含有Ag+、Fe3+、K+、Ba2+、NH4+等离子,进行如下实验:
(1)加入过量的稀盐酸,有白色沉淀产生;(2)过滤,在滤液中加入过量的稀硫酸,又有白色沉淀生成;(3)过滤,取少量滤液,滴入2滴KSCN溶液,没有明显的现象出现;(4)另取少量步骤(3)中的滤液,加入NaOH溶液至溶液显碱性,加热,可产生使湿润的红色石蕊试纸变蓝色的气体。
根据实验现象回答:待测液中一定含有 离子,一定不含有 离子,还有一种离子不能确定是否存在,要检验这种离子的实验方法是(只填写实验名称和观察到的现象)
过氧化钠是一种淡黄色固体,它能与二氧化碳反应生成氧气,在潜水艇中用作制氧剂,供人类呼吸之用.它与二氧化碳反应的化学方程式为: 2Na2O2 + 2CO2 ="=" 2Na2CO3 + O2。某学生为了验证这一实验,以足量的大理石、足量的盐酸和1.95g过氧化钠样品为原料,制取O2,设计出如下实验装置:
(1)A中制取CO2 的装置,应从下列图①和②中选哪个图:
B装置的作用是,C装置内出现的现象是。为了检验E中收集到的气体,在取出集气瓶后,用的木条伸入集气瓶内,木条会出现。
(2)若E中的石灰水出现出现轻微白色浑浊,请说明原因:。
(3)反应完毕时,若测得E中的集气瓶收集到的气体250毫升,又知氧气的密度为1.43克/升,当装置的气密性良好的情况下,实际收集到的氧气体积比理论计算值(偏大或偏小),相差约毫升(取整数值,所用数据均在标准状况下测定),这可能是由于。
(4)你认为上述A---E的实验装置中,E部分是否安全、合理?
E是否需要改进,若需要改进,应改为下图中的(填甲、乙、丙、丁).
(本小题14分:每空2分)下图是实验室制备氯气并进行一系列相关实验的装置(夹持设备已略)。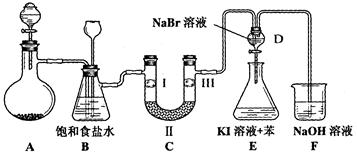
(1)制备氯气选用的药品为:漂粉精固体和浓盐酸,相关的化学反应方程式为:____。
(2)装置B中饱和食盐水的作用是_________________________________;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象__________。
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入___。
| A |
B |
C |
D |
|
| Ⅰ |
干燥的有色布条 |
干燥的有色布条 |
湿润的有色布条 |
湿润的有色布条 |
| Ⅱ |
碱石灰 |
硅胶 |
浓硫酸 |
无水氯化钙 |
| Ⅲ |
湿润的有色布条 |
湿润的有色布条 |
干燥的有色布条 |
干燥的有色布条 |
(4)设计装置D、E的目的是。打开活塞,将装置D中少量溶液加入装置E中,振荡。观察到的现象是_______________________________。
(5)某同学建议将装置F中的药品改用足量的NaHSO3溶液吸收余氯,老师认为不妥,用总反应的离子方程式解释原因_____________________________________。
某校化学实验兴趣小组欲采用如图所示的实验装置制Cl2,同时进行与氯气有关的某些实验,按要求回答问题。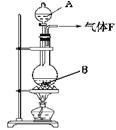
(1)药品A的名称是,此反应的离子方程式是。
(2)甲同学用含有0.2 mol HCl的浓盐酸与足量的MnO2反应制Cl2,结果制得的Cl2体积(标准状况下)1.12 L(填“大于”“等于”“ 小于”)。
(3)在实验室中,乙同学欲用下图中的装置净化氯气,则气流方向是:
气体F→ → → → (填代号)。
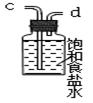
(4)把净化后的氯气通入如下图装置。
①观察到a不褪色,b褪色,可得到的结论是:;②检验吸收Cl2后的NaOH溶液中含有Cl-时,需要滴加的试剂以及现象为。
(5)一位同学设计了一套用浓盐酸和KMnO4固体制取少量氯气并比较氯气与碘单质的氧化性强弱的微型装置(如图)。
能说明Cl2的氧化性强于I2的实验现象是:。
某学生用0.1000 mol·L-1的NaOH标准溶液滴定未知浓度的盐酸,其操作可分解为如下几步:
A.移取20 mL待测盐酸溶液注入洁净的锥形瓶,并加入2~3滴酚酞;
B.用标准溶液润洗滴定管2~3次;
C.把盛有标准溶液的碱式滴定管固定好,调节滴定管尖嘴使之充满溶液;
D.取标准NaOH溶液注入碱式滴定管至刻度0以上2~3 cm;
E.调节液面至0或0以下刻度,记下读数;
F.把锥形瓶放在滴定管的下面,用标准NaOH溶液滴定至终点并记下滴定管液面的刻度。
就此实验完成填空:
(1)正确操作步骤的顺序是(用序号字母填写)______________________________。
(2)上述B步骤操作的目的是_______________________________________。
(3)实验中用左手控制活塞,眼睛注视___________________,直至滴定终点。判断到达终点的现象是________________________________。
(4)某学生根据3次实验分别记录有关数据如下表:
| 滴定 次数 |
待测溶液的体积(mL) |
0.100 0 mol·L-1NaOH的体积(mL) |
||
| 滴定前刻度 |
滴定后刻度 |
溶液体积(mL) |
||
| 第一次 |
20.00 |
0.00 |
26.11 |
26.11 |
| 第二次 |
20.00 |
1.56 |
30.30 |
28.74 |
| 第三次 |
20.00 |
0.22 |
26.31 |
26.09 |
依据上表数据列式计算该盐酸溶液的物质的量浓度为
(5)用0.1000 mol·L-1 NaOH溶液滴定0.1000 mol·L-1盐酸,如达到滴定的终点时不慎多加了1滴NaOH溶液(1滴溶液的体积约为0.05 mL),继续加水至50 mL,所得溶液的pH等于____________
(6)下列哪些操作会使测定结果偏高(填序号)。
A.锥形瓶中溶液的颜色刚刚由无色变为浅红色即停止滴定
B.碱式滴定管用蒸馏水洗净后立即注入标准液
C.滴定前碱式滴定管尖端气泡未排除,滴定后气泡消失
D.滴定前读数正确,滴定后俯视滴定管读数
E.实验中,用待盛装的溶液润洗锥形瓶
(18分)一氯甲烷,也叫甲基氯,常温下是无色气体,密度为0.9159g/cm3,熔点为-97.73℃,沸点为-24.2℃,18℃时在水中的溶解度为280mL/mL水,与乙醚、丙酮或苯互溶,能溶于乙醇。在实验室里可用下图装置制造一氯甲烷: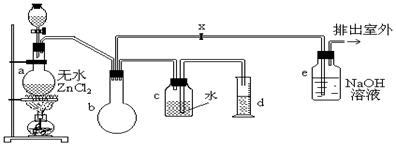
制备装置的分液漏斗和烧瓶中分别盛有甲醇和浓盐酸。
试填写下列空白:
(1)制备一氯甲烷的化学方程式,其反应类型属于反应;
(2)装置b的作用是;
(3)已知卤代烃能发生碱性水解,转化为醇。装置e中可能发生的反应方程式为;
(4)检验气体产物CH3Cl的方法是:在e的逸出口点燃CH3Cl气体,火焰呈蓝绿色(与其它烃燃烧现象有明显区别)。CH3Cl燃烧的化学方程式是;
(5)实验中实际按甲醇和浓盐酸1︰2(物质量之比)进行反应的理由是;
(6)某学生在关闭活塞x的情况下做此实验时发现,收集到一定体积的气体产物所消耗的甲醇~
浓盐酸的混和液的量比正常情况下多(装置的气密性没有问题),其原因是;
(7)实验结束后,d中收集到的液体中含有。