铅蓄电池是可充电型电池,它的正负极极板是惰性材料,电池总反应式为:
Pb+PbO2+4H++2SO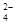
 2PbSO4+2H2O
2PbSO4+2H2O
请回答下列问题(不考虑氢、氧的氧化还原):
(1) 该蓄电池放电工作时的负极材料是 ,用其电解氯化钠溶液,当阳极上收集到11.2L氯气时(标况下),理论上负极板的质量增加 g。
充电时,上图中A极应接直流电源的 (填“正极”或“负极”)。充电时A极的电极反应式是 ;
(2) MnO2的生产方法之一是以石墨为电极,电解酸化的MnSO4溶液。阴极的电极反应式 。现以铅蓄电池为电源电解,当蓄电池中有0.4mol H+被消耗时,则电路中通过的电子的物质的量为 ,MnO2的理论产量为 g。
(4分)将下列物质进行分类(填序号)
① O2与O3②126C与136C③冰与水
④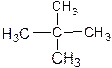 和
和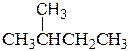
(1)互为同位素的是(2)互为同素异形体的是
(3)互为同分异构体的是(4)属于同一化合物的是
写出下列物质的结构式
①CH4_____________②NH3__________③ Cl2_____________
写出下列物质或微粒的电子式
① HNa+Cl-
②H2OHClMgCl2
指出下列元素在周期表中的位置:
①Ne:周期族;②C:周期族;
③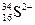 微粒中的质子数是_______,中子数是_______,核外电子数是_______。
微粒中的质子数是_______,中子数是_______,核外电子数是_______。
据报道,卫生部决定从2011年5月1日起禁用面粉增白剂。资料显示,目前应用于面粉的增白剂几乎全是过氧化苯甲酰,它能对面粉起到漂白和防腐的作用,且已经过安全评估,但是有研究认为它对人体有一定的负面作用。过氧化苯甲酰的合成路线如下: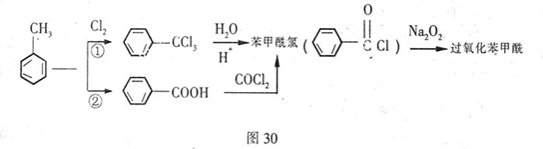
(1)过氧化苯甲酰的组成元素仅为C、H、O,其中含氧质量分数为26.45%,相对分子质量为242,通过计算和推理可知,过氧化苯甲酰的分子式为,结构简式为。
(2)反应①、②的反应类型分别为和,反应①所需的条件为。
(3)苯甲酸有多种同分异构体,其中属于芳香族化合物有种(不含苯甲酸)。
(4)苯甲酰氯也有多种同分异构体,其中邻氯苯甲醛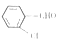 可用于制备一种重要的有机化工原料水杨酸
可用于制备一种重要的有机化工原料水杨酸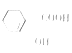 ,使用流程图表示其制备过程。
,使用流程图表示其制备过程。
(流程图示例如下:CH3CH2OH H2C=CH2
H2C=CH2 BrH2CCH2Br)
BrH2CCH2Br)