生产、生活中广泛使用着金属及金属材料。
(1)金属钛(Ti)及钛的合金被认为是21世纪重要的金属材料。地壳中的钛主要以氧化物的形式存在,其中钛元素的化合价是+4价,该氧化物的化学式为 。
(2)防止铁制品锈蚀需要了解铁锈蚀的条件。铁锈蚀的条件是 。
(3)实验室废液中含有硝酸银、硝酸铜,实验小组利用稀硫酸和铁粉分别回收银和铜,设计如下方案。
先在废液中加入过量的铁粉,充分反应后过滤得到滤渣A,其成分为____。再对滤渣A按如下流程图处理: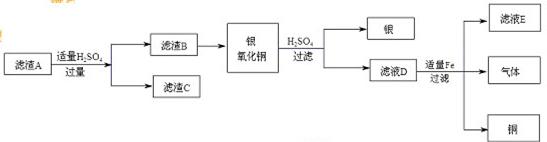
①先再废液中加入过量的铁粉,过量的目的是 。
②含有硫酸亚铁的滤液有 (填框图中字母)。
③如果在过滤操作中发现滤液浑浊,在仪器洁净、滤纸未破损的前提下,你认为滤液的浑浊的原因可能是 。
钙是一种非常活泼的金属,常温下能与水发生反应,反应的化学方程式为:Ca+2H2O═Ca(OH)2+H2↑.在实验室,某兴趣小组先将一定量的硫酸铜溶液倒入烧杯中,再取一块钙加入到硫酸铜溶液中,观察到有大量气泡产生,同时有蓝色沉淀生成。充分反应后过滤,得到滤液和蓝色滤渣,兴趣小组对滤渣的成分进行探究。
[提出问题]滤渣的成分是什么?
[查阅资料]Ca(OH)2微溶于水,Cu(OH)2不溶于水。
[猜想与假设]猜想一:全部是Ca(OH)2
猜想二:全部是Cu(OH)2
猜想三:
小东从物理性质进行分析后认为猜想 不合理,理由是 。
[实验与验证]
|
实验 |
实验操作 |
实验现象 |
实验结论 |
|
实验Ⅰ |
取少量蓝色滤渣放入烧杯中,加入适量的水溶解后过滤,将滤液分成两等份,向其中一份滴入酚酞试液 |
滴入酚酞后滤液 呈 色 |
滤液显碱性,证明滤液中有OH﹣离子 |
|
实验Ⅱ |
向实验Ⅰ的另一份滤液中滴入Na2CO3溶液 |
有白色沉淀 |
证明滤液中有 离子 |
[结论与反思]根据实验Ⅰ和实验Ⅱ可以证明猜想 正确,写出实验Ⅱ中发生反应的化学方程式 。
[拓展与延伸]Na和Ca都是非常活泼的金属,都能与O2反应生成过氧化物。这两种过氧化物与水反应的化学方程式分别为:2Na2O2+2H2O═4NaOH+O2↑和2CaO2+2H2O═2Ca(OH)2+O2↑.长途运输鱼苗时常选择CaO2作供氧剂而不选择Na2O2的原因是 。
化学是一门以实验为基础的学科。请结合下列实验装置图回答问题:
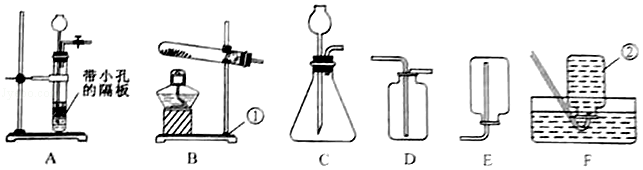
(1)写出图中①、②两种仪器的名称:① ,② 。
(2)某同学用高锰酸钾加热制取氧气,反应的化学方程式为 ;应选择的发生装置为 (填字母) ,收集装置为 (填字母)。
(3)A装置与C装置比较,A装置的优点是可以控制反应的发生和停止。请写出一个利用A装置此优点的反应化学方程式 。
(4)实验室可用金属与浓硫酸反应制取SO2气体,金属锌和金属铜都能与浓硫酸反应制SO2气体。欲制取一瓶纯净的SO2气体,最好选择金属 (填“锌”或“铜”),选择理由是 。
华为公司作为我国高科技的代表,一直致力于核心技术的开发。2019年,华为公司推出了5G商用芯片。制造芯片需要用到高纯硅,工业上利用二氧化硅制备高纯硅的工艺流程如图:

(1)写出CO的任意一点物理性质 。
(2)写出反应③的化学方程式 ,该反应属于 (填基本反应类型)反应。
(3)玻璃的主要成分是二氧化硅,二氧化硅属于 (填“金属氧化物”或“非金属氧化物”)。二氧化硅(SiO2)与氢氧化钠溶液反应类似于二氧化碳与氢氧化钠溶液的反应。请写出二氧化硅与氢氧化钠溶液反应的化学方程式 。
(4)整个制备过程必须在无水、无氧气的环境中进行,原因是 。
元素周期表是学习和研究化学的重要工具。如图是元素周期表的一部分,元素周期表的横行叫做周期,纵行叫做族,分为主族、副族、ⅤⅢ族和0族,主族用字母A表示,共有七个主族,依次用ⅠA、ⅡA……表示,同一主族元素化学性质相似。根据表回答问题:
|
族/周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
VⅥA |
ⅧA |
0 |
|
一 |
1 H 氢 |
2 He 氦 |
||||||
|
二 |
3 Li 锂 |
4 Be 铍 |
5 B 硼 |
6 C 碳 |
7 N 氮 |
8 O 氧 |
9 F 氟 |
10 Ne 氖 |
|
三 |
11 Na 钠 |
12 Mg 镁 |
13 Al 铝 |
14 Si 硅 |
15 P 磷 |
16 S 硫 |
17 Cl 氯 |
18 Ar 氩 |
(1)观察元素周期表,可发现同一周期接近尾部的是 (填“金属”或“非金属”)元素,在化学反应中容易 (填“得到”或“失去”)电子。
(2)根据元素周期表可以查到第三周期、第ⅡA族的元素是 ,它的原子序数为 。
(3)氯离子(Cl﹣)的质子数是17,则氧离子的核外电子总数为 。
(4)在元素周期表中,He元素不排在ⅡA族而排在0族的依据是 。
赤铁矿是一种常见的铁矿石,赤铁矿主要成分是 。在高温条件下用碳还原赤铁矿冶炼成铁,同时产生CO、CO2混合气体,此混合气体中碳的质量分数为40%,请写出该反应的化学方程式 。