下表列出了①~⑥六中元素在周期表中的位置:
族 周期 周期 |
ⅠA |
|
|
|
0 |
|||
| |
||||||||
| 1 |
|
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
|
| 2 |
① |
|
|
② |
③ |
|
|
|
| 3 |
④ |
|
⑤ |
|
|
|
⑥ |
|
请按要求回答下列问题:
(1)写出下列标号元素的元素符号:① 、⑤ 。
(2)④和⑥两种元素形成的化合物的电子式是 。
(3)元素②形成的最简单有机物的空间结构为 。
(4)元素④的单质在氧气中燃烧的化学方程式是 。
(6 分)某研究学习小组在做过氧化钠与水反应实验时,发现过氧化钠与水反应后的溶液滴加酚酞呈红色,但不久红色褪去。甲、乙、丙三个同学对此现象分别做了如下推测:
甲:因为反应后试管很热,所以很可能是溶液温度较高使红色褪去。
乙:查阅资料上载“酚酞在浓的碱溶液中因生成三钠盐而呈无色。”实验所加的水较少,红色褪去可能是生成的氢氧化钠溶液浓度较大的影响。
丙:过氧化钠具有强氧化性,生成物中O2 、H2O2(可能产物)等也具有强氧化性,可能是氧化漂白了红色物质。
(1)验证甲是否正确的方法是_________________________
(2)验证乙是否正确的方法是_________________________
将下列离子Na+、K+、Cu2+、H+、NO3-、Cl-、CO32-、OH-按可能大量共存于同一溶液的情况,把他们分成A、B两组,而且每组中均含两种阳离子和两种阴离子。
A组:
B组:
过氧化氢H2O2,(氧的化合价为-1价),俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。对于下列A~D涉及H2O2的反应,填写空白:
| A.Na2O2 +2HCl= 2NaCl+H2O2 | B.Ag2O+ H2O2=2Ag+O2+ H2O |
| C.2 H2O2="2" H2O+O2 | D.3 H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8 H2O |
(1)H2O2仅体现氧化性的反应是(填代号)。
(2)H2O2既体现氧化性又体现还原性的反应是(填代号)。
(3)H2O2体现酸性的反应是(填代号)。
(4)上述反应说明H2O2、Ag2O、K2CrO4氧化性由强到弱的顺序是:。
(8分)提示:某些金属氧化物跟熔融烧碱反应可生成盐。根据以下化学反应框图填空: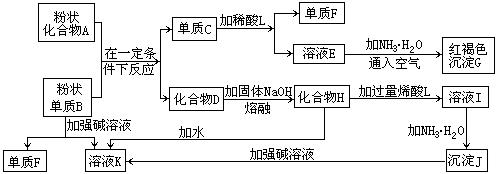
(1)单质F是_____________________。
(2)写出由E生成G的离子反应方程式(或化学方程式)________________________。
(3)溶液I中所含金属离子是_____________________。
(4)由C→E+F若改用浓酸,则不能选用的浓酸是(写分子式)____________________。
(10分)(2004年天津高考题)锌和铝都是活泼金属,其氢氧化物既能溶于强酸,又能溶于强碱。但是氢氧化铝不溶于氨水,而氢氧化锌能溶于氨水,生成Zn(NH3)42+。回答下列问题:
(1)单质铝溶于氢氧化钠溶液后,溶液中铝元素的存在形式为(用化学式表示)。
(2)写出锌和氢氧化钠溶液反应的化学方程式。
(3)下列各组中的两种溶液,用相互滴加的实验方法即可鉴别的是。
①硫酸铝和氢氧化钠②硫酸铝和氨水
③硫酸锌和氢氧化钠④硫酸锌和氨水
(4)写出可溶性铝盐与氨水反应的离子方程式。
试解释在实验室不适宜用可溶性锌盐与氨水反应制备氢氧化锌的原因。