根据右表提供的数据,判断在等浓度的NaCN、NaHS混合溶液中,各种离子浓度关系正确的是:
| 化学式 |
电离常数 |
| HCN |
k=4.93×10-10 |
| H2S |
K1=9.1×10-8 |
| K2=1.1×10-12 |
A.c(CN-)>c(HS-)>c(OH-)
B.c(HS-)>c(CN-)>c(H+)
C.c(Na+)+c(H+)=c(HS-)+ c(CN-)+ c(OH-)
D.c(HCN)+c(CN-)=c(HS-)+ c(H2S)
北京奥运会期间对大量盆栽鲜花施用了S-诱抗素制剂,以保证鲜花盛开。S-诱抗素的分子结构如下图,下列关于该物质的说法正确的是( )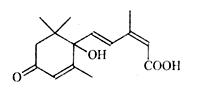

A.含有碳碳双键、羟基、羰基、羧基 |
B.含有苯环、羟基、羰基、羧基 |
C.含有羟基、羰基、羧基、酯基 |
D.含有碳碳双键、苯环、羟基、羰基 |
每年的6月26日是国际禁毒日,珍爱生命,远离毒品。以下是四种毒品的结构简式,下列有关说法正确的是( )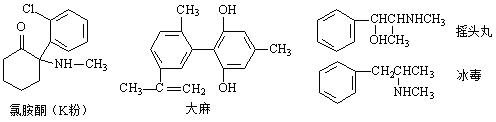
| A.四种毒品都属于芳香族化合物,都难溶于水 82615205 |
B.摇头丸和冰毒互为同分异构体 |
C.1mol大麻与溴水反应最多消耗4mol Br2 |
| D.大麻分子中所有碳原子不可能共平面 |
以下各组物质可以用分液漏斗分离的是 ( )
| A.硝基苯和水 | B.乙醇和水 |
| C.甲醛和水 | D.乙酸乙酯和乙酸 |
下列分子式表示的物质一定是纯净物的是( )
A.C5H1 0 0 |
B.C2H4O2 | C.CH4O | D.C2H4Cl2 |
把氢氧化钠溶液和硫酸铜溶液加入到某病人的尿液微热,如果观察到红色沉淀说明尿液中含有( ):
| A.食醋 | B.白酒 | C.食盐 | D.葡萄糖 |