化学电池在通讯、交通及日常生活中有着广泛的应用,目前常用的镍(Ni)镉(Cd)电池,其电池总反应可示为: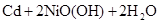

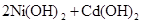
(1)下列有关镍镉电池总反应的说法中,正确的是________(填序号);
①以上反应是可逆反应 ②以上反应不是可逆反应
③充电时化学能转变为电能 ④放电时化学能转变为电能
(2)已知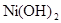 和
和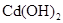 均难溶于水.有资料表明,一节废镍镉电池可以使一平
均难溶于水.有资料表明,一节废镍镉电池可以使一平
方米面积的耕地失去使用价值,在酸性土壤中这种污染尤为严重.这是因为_ __
_____________________________________;
(3)另一种常用的电池是锂电池(锂是一种碱金属元素,其相对原子质量为7),由于它的比容量(单位质量电极材料所能转换的电量)特别大而广泛应用于心脏起搏器,一般使用时间可长达十年.电池总反应可表示为: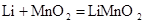 .试回答:①锂电池比容量特别大的原因是_______________________________________;
.试回答:①锂电池比容量特别大的原因是_______________________________________;
②锂电池中的电解质溶液需用非水溶剂配制,为什么这种电池不能使用电解质的水溶液?请用化学方程式表示其原因_______________________________________.
四川北川盛产蔷薇科植物。蔷薇科植物中含有一种芳香醛(用E表示),在染料工业和食品工业上有着广泛的用途,下面是它的一种合成路线。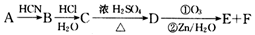
其中0 . l mol有机物A的质量是 12g ,在足量的氧气中充分燃烧后生成0.8mol CO2和 7.2gH2O; D 能使溴的四氯化碳溶液褪色, D 分子与 C 分子具有相同的碳原子数;F继续被氧化生成G,G 的相对分子质量为 90 。
已知: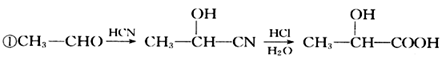

回答下列问题:
(1)A 的结构简式为__________________。
(2)A~G中能发生酯化反应的有机物有:(填字母序号)。
(3)C在浓硫酸加热的条件下时,分子内脱水除生成D外还可以生成另一种有机物,写出该反应的方程式:;该反应类型;
(4)C 的同分异构体有多种,其中符合下列要求的有机物有多种。
①能与3 mol NaOH溶液反应;
②苯环上的一卤代物只有一种
写出所有满足条件有机物的结构简式______________________________
(5)C与4-甲基-2,3-戊二醇两分子之间1:1发生取代反应,生成的有机物有种。
(1)一定温度下,向1 L 0.1 mol·L-1 CH3COOH溶液中加入0. 1 mol CH3COONa固体,则醋酸的电离平衡向________(填“正”或“逆”)反应方向移动;溶液中 的值________(填“增大”、“减小”或“不变”)。
的值________(填“增大”、“减小”或“不变”)。
(2)氨气的水溶液称为氨水,其中存在的主要溶质微粒是NH3·H2O。
已知:a.常温下,醋酸和NH3·H2O的电离平衡常数均为1.74×10-5;
b.CH3COOH+NaHCO3===CH3COONa+CO2↑+H2O。
则CH3COONH4溶液呈________性(填“酸”、“碱”或“中”,下同),NH4HCO3溶液呈________性,NH4HCO3溶液中物质的量浓度最大的离子是________(填化学式)。
(3)99 ℃时,Kw=1.0×10-12,该温度下测得0.1 mol·L-1 Na2A溶液的pH=6。
①H2A在水溶液中的电离方程式为___________________。
②该温度下,将0.01 mol·L-1 H2A溶液稀释到20倍后,溶液的pH=________。
③体积相等、pH=1的盐酸与H2A溶液分别与足量的Zn反应,产生的氢气________。
| A.盐酸多 | B.H2A多 | C.一样多 | D.无法确定 |
④将0.1 mol·L-1 H2A溶液与0.2 mol·L-1氨水等体积混合,完全反应后溶液中各离子浓度从大到小的顺序为_____________________。
(1)实验室里常用浓盐酸与二氧化锰反应来制取少量的氯气,反应的化学方程式为:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O,取一定量的浓盐酸使其与二氧化锰发生反应,产生的氯气在标准状况下的体积为22.4 L。请回答下列问题:
MnCl2+Cl2↑+2H2O,取一定量的浓盐酸使其与二氧化锰发生反应,产生的氯气在标准状况下的体积为22.4 L。请回答下列问题:
①写出该反应的离子反应方程式________________,
②反应中被氧化的HCl的物质的量为________mol。
③实验室备用的浓盐酸质量分数为36.5%,密度为1.19 g·cm-3,为使用方便,请计算出该浓盐酸的物质的量浓度_________ molL-1。
(2)把一小块镁铝合金溶于100mL盐酸中,然后向其中滴入1 molL-1NaOH溶液,生成沉淀的质量和加入NaOH溶液的体积如下图所示。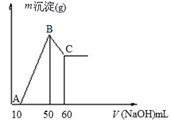
①合金中镁的质量g。
②盐酸的物质的量浓度molL-1
姜黄素具有防肿瘤的作用,工业上可以通过中间体E合成。
I合成中间体E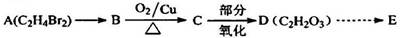
(1)A→B的反应方程式为____。
(2)D的官能团名称为;c中处于同一平面上的原子最多个。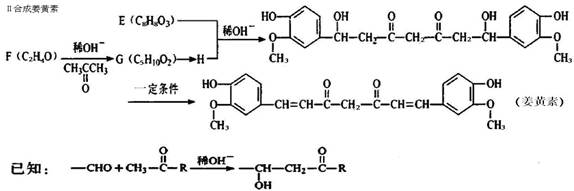
(3)F—→G的化学方程式为;G→H的反应类型为。
(4)中间体E的结构简式为;
将F滴人新制Cu(OH)2悬浊液,加热,观察到的现象是____。
(5)写出所有符合下列条件的E的同分异构体的结构简式。
①能与N a反应 ②苯环上一卤代物只有一种 @含﹥c= c﹤
某叶绿素的化学式为C55 H72N4O6Mg,其在人体代谢的中间产物为CO( NH:2)20。
(1)该叶绿素所含元素中,基态原子第一电离能最大的是(填元素符号,下同);处于s区的元素有。
(2)已知CO( NH2)2分子中C、N、O原子均达8电子稳定结构,其中N的杂化轨道类型为;在CO(NH2)2晶体中存在____(填序号)o
A.非极性键B.极性键C.氢键D.范德华力
(3)CO(NH2)2的熔点远远低于NaCl.其原因是。
(4)工业上,用惰性电极电解法除去碱性溶液中的CO( NH2)2,产物均为无毒无害常见物质。则阳极除去CO(NH2)2的电极反应式为。