铅蓄电池是典型的可充型电池,它的正负极格板是惰性材料,电池总反应式为:
Pb+PbO2+4H++2SO2-4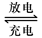 2PbSO4+2H2O
2PbSO4+2H2O
请回答下列问题(不考虑氢、氧的氧化还原):
(1)放电时:正极的电极反应式是______________;电解液中H2SO4的浓度将变________;当外电路通过1mol电子时,理论上负极板的质量增加________g。
(2)在完全放电耗尽PbO2和Pb时,若按右图连接,电解一段时间后,则在A电极上生成__________、B电极上生成________,此时铅蓄电池的正负极的极性将__________________。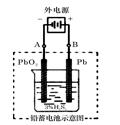
反应A+3B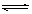 2C+2D在四种不同情况下的反应速率分别为:
2C+2D在四种不同情况下的反应速率分别为:
①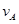 =0.15mol/(L·min)②
=0.15mol/(L·min)②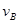 =0.01mol/(L·s)
=0.01mol/(L·s)
③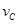 =0.40mol/(L·min) ④
=0.40mol/(L·min) ④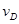 =0.45mol/(L·min),
=0.45mol/(L·min),
该反应进行的快慢顺序为(填序号)。
已知反应4NH3(g)+5O2(g)==4NO(g)+6H2O(g)在10L密闭容器中进行,半分钟后,水蒸气的物质的量增加了4.5mol,试计算分别用NH3、O2、NO、H2O四种不同物质表示的该反应的反应速率。
将氮气、氢气的混合气体分别充入甲、乙、丙三个容器中进行合成氨反应,经过一段时间后,反应速率为:甲:v (H2)=3mol/(L· min);乙:v (N2) =2mol/(L·min);丙: v (NH3)= 1mol/(L·min),则这段时间内三个容器中反应速率由大到小的顺序是。
根据以下叙述回答。
能源可划分为一级能源和二级能源。自然界中以现成形式提供的能源称为一级能源;需依靠其他能源的能量间接制取的能源称为二级能源。氢气是一种高效而没有污染的二级能源,它可以由自然界中大量存在的水来制取:
(1)下列叙述正确的是()
A.电能是二级能源B.水力是二级能源
C.天然气是一级能源D.水煤气是一级能源
(2)关于用水制取二级能源氢气,以下研究方向不正确的是()
A.构成水的氢和氧都是可以燃烧的物质,因此可研究在水不分解的情况下,使氢成为二级能源
B.设法将太阳光聚焦,产生高温,使水分解产生氢气
C.寻找高效催化剂,使水分解产生氢气,同时释放能量
D.寻找特殊化学物质,用于开发廉价能源,以分解水制氢气
(3)1g氢气燃烧时约放热142.9kJ,而1kg汽油燃烧时约放热46000kJ。氢气被公认是21世纪替代矿物燃料的理想能源。你认为氢气作为能源的三个主要优点:_______________,________________,________________。
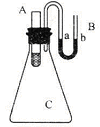
如图所示,在锥形瓶放置有装有水的小试管,往小试管中分别加入下列物质时:①烧碱固体②浓硫酸③硝酸铵固体④NaCl固体,其中能使a端液面高于b端液面的是__________________。(填序号)