金属晶体具有延展性的原因( )
| A.金属键很微弱 |
| B.金属键没有饱和性 |
| C.密堆积层的阳离子容易发生滑动,但不会破坏密堆积的排列方式,也不会破坏金属键 |
| D.金属阳离子之间存在斥力 |
在体积为VL的恒容密闭容器中盛有一定量H2,通入Br2(g)发生反应:H2(g)+Br2(g) 2HBr(g);ΔH<0。当温度分别为T1、T2平衡时,H2的体积分数与Br2(g)的物质的量变化关系如图所示。下列说法正确的是
2HBr(g);ΔH<0。当温度分别为T1、T2平衡时,H2的体积分数与Br2(g)的物质的量变化关系如图所示。下列说法正确的是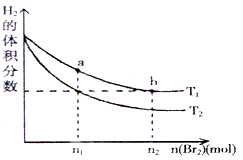
| A.由图可知:T2>T1 |
| B.两点的反应速率:a>b |
| C.T1时,随着Br2(g)加入,平衡时HBr的体积分数不断增加 |
| D.a点比b点体系的颜色深 |
用下列物质冶炼金属的过程中,需要加入还原剂的是
| A.Fe2O3 | B.Al2O3 | C.HgO | D.Cu2S |
下列关于化学平衡常数的说法中错误的是
| A.化学平衡常数K只与温度有关,随温度的升高,K可能增大、减小或不变 |
| B.催化剂不能改变平衡常数的大小 |
| C.若某一条件的改变,使平衡常数发生了变化,则化学平衡必发生移动 |
| D.化学平衡移动时,平衡常数必改变 |
下列事实不能用勒沙特列原理解释的是
A.合成氨反应:N2(g)+3H2(g) 2NH3(g) ;△H<0,为使氨的产率提高,理论上应采取低温高压的措施 2NH3(g) ;△H<0,为使氨的产率提高,理论上应采取低温高压的措施 |
|
B.对2HI(g) H2(g)+I2(g)平衡体系增加压强使颜色变深 H2(g)+I2(g)平衡体系增加压强使颜色变深 |
|
| C.使用催化剂有利于提高SO2与O2生成SO3的效率 |
D.用排饱和氯化钠溶液的方法来收集氯气 |
汽车的启动电源常用铅蓄电池,该电池在放电时的反应如下:PbO2 (s)+Pb(s)+2H2SO4(aq)===2PbSO4(s)+2H2O(l),根据此反应判断下列叙述中正确的是
| A.PbO2是电池的负极 |
| B.负极的电极反应式为:Pb(s)+SO42-(aq)–2e – = PbSO4(s) |
| C.铅蓄电池属于一次性电池 |
| D.电池放电时,溶液酸性增强 |