人造地球卫星用到的一种高能电池——银锌蓄电池,它在放电时的电极反应为:
Zn + 2OH– –2e–=ZnO + H2O,Ag2O + H2O + 2e–=2Ag + 2OH–,据此判断氧化银是
| A.负极,并被氧化 | B.正极,并被还原 |
| C.负极,并被还原 | D.正极,并被氧化 |
短周期主族元素X、Y、Z、M、W在元素周期表中的相对位置如图,其中Z的核电荷数是Y 的两倍.下列说法正确的是
| A.M位于元素周期表中第三周期ⅣA族 |
| B.原子半径:Z>M>X |
| C.气态氢化物的热稳定性:Y>X>W |
| D.W的氧化物既能与NaOH反应,也能与HF反应,属于两性氧化物 |
如图所示,两圆圈相交的阴影部分表示圆圈内的物质相互发生的反应.已知钠及其氧化物的物质的量均为0.1 mol,水的质量为100 g.。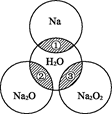
下列说法正确的是
| A.Na2O2晶体中阴阳离子数目之比为1∶1 |
| B.反应③最多能产生0.05 mol O2 |
| C.反应①的离子方程式为Na+2H2O==Na++2OH-+H2↑ |
| D.①、②、③充分反应后所得溶液的质量分数从大到小的顺序为①>②>③ |
下列各组离子能在指定溶液中大量共存的是
①无色溶液中:Al3+、Cl-、Na+、HCO3-、SO42-
②pH=11的溶液中:Na+、AlO2-、NO3-、S2-、SO32-
③加入Mg能放出H2的溶液中:Mg2+、NH4+、Cl-、K+、SO42-
④使pH试纸呈红色的溶液中:Fe3+、MnO4-、Na+、SO42-
⑤酸性溶液中:Fe2+、Al3+、NO3-、I-
| A.①②④ | B.①⑤ | C.②③④ | D.①②③ |
用NA表示阿伏加德罗常数,下列说法正确的是
| A.500mL2mol/L葡萄糖溶液中所含分子数为NA |
| B.0.1mol/L Na2CO3溶液中的阴离子总数大于0.1NA |
| C.电解精炼铜时,若阳极质量减少64g,则外电路导线上不一定通过2NA个电子 |
| D.5.6g铁粉在0.1mol氯气中充分燃烧,转移电子数为0.3NA |
能用如图气体制取装置制取少量气体并能“随开随用、随关随停”的是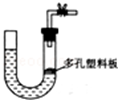
| A.大理石和稀硫酸制取二氧化碳 |
| B.锌粒和稀硫酸制氢气 |
| C.浓盐酸和二氧化锰制取氯气 |
| D.过氧化钠和水制取氧气 |