a mol乙炔跟b mol氢气在密闭容器中反应,当其达到平衡时,生成c mol乙烯,将平衡混合气体完全燃烧生成CO2和H2O,所需氧气的物质的量是
A. mol mol |
B. mol mol |
C. mol mol |
D. mol mol |
有一处平衡状态的反应2X(s)+Y(g)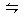 2Z(g)△H<0。为了使平衡向生成Z的方向移动,应采取的措施是()
2Z(g)△H<0。为了使平衡向生成Z的方向移动,应采取的措施是()
①升高温度;②降低温度;③增大压强;④减小压强;⑤加入催化剂;⑥及时分离出Z。
| A.①③⑤ | B.②③⑤ | C.②③⑥ | D.②④⑥ |
合成氨需要的H2由煤和水反应制得,其中一步反应为:CO(g)+H2O(g)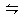 CO2(g)+H2(g)△H>0,要使CO转化率提高,可采取()
CO2(g)+H2(g)△H>0,要使CO转化率提高,可采取()
| A.增大H2O(g)的浓度 | B.增大CO的浓度 |
| C.降低温度 | D.增大压强 |
在合成氨工业中,为增加NH3的日产量,实施下列目的的变化过程中与平衡移动无关的是()
| A.不断将氨分离出来 | B.使用催化剂 |
| C.采用500℃左右的高温 | D.采用2×107~5×107Pa的压强 |
可逆反应N2+3H2 2NH3 △H<0,达到平衡后,为使H2的转化率增大,下列说法正确的是()
2NH3 △H<0,达到平衡后,为使H2的转化率增大,下列说法正确的是()
| A.升高温度,降低压强,增加氮气 |
| B.降低温度,增大压强,加入催化剂 |
| C.升高温度,增大压强,增加氮气 |
| D.降低温度,增大压强,分离部分氨 |
工业上用氨和二氧化碳反应合成尿素。已知下列物质在一定条件下均能与水反应产生H2和CO2,H2是合成氨的原料,CO2供合成尿素使用。若从充分利用原料的角度考虑,最好选用的原料是()
| A.CO | B.石脑油(C5H12、C6H14) | C.CH4 | D.焦碳 |