(共12分)实验室里通常用MnO2与浓盐酸在加热的条件下反应制取氯气,为进行有关氯气的性质实验,需要4瓶容积为100ml的氯气(标准状况)。
(1)写出实验室制取氯气的化学反应方程式并标出电子转移的方向及数目。
(2)制取4瓶氯气,理论上需要MnO2固体的质量是多少?(浓盐酸过量,并可以补充)
(3)实际称量的MnO2固体的质量必需多于理论量,主要原因是什么?
(1)2 s 时体系内的压强为开始时压强的多少倍?
(2)平衡体系中含N2O4的物质的量为多少?
(3)问2 s时以N2O4的浓度表示的平均反应速率是多少?
已知:N2(g)+3H2(g) 2NH3(g);ΔH="-92.4" kJ·mol-1。请回答:
2NH3(g);ΔH="-92.4" kJ·mol-1。请回答:
(1)合成氨工业中采取的下列措施可以用勒夏特列原理解释的是(填字母)。
a.用铁触媒加快化学反应速率 b.采用较高压强(20MPa~50MPa)
c.将原料气中的少量CO等气体净化除去d.将生成的氨液化并及时从体系中分离出来
(2)一定温度下,在密闭容器中充入1 mol N2和3 mol H2并发生反应。若容器容积恒定,达到平衡时,气体的压强为原来的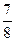 ,则N2的转化率a1=,此时,反应放热kJ;
,则N2的转化率a1=,此时,反应放热kJ;
室温时,若0.1mol·L-1NaX溶液的pH=9,该溶液中发生水解反应的X-占全部X-的物质的量分数为多少?
(6分)在一支10mL试管中充满NO2和O2的混合气体,将其倒立于盛满足量水的水槽中。若x表示原混合气体中NO2的体积(mL),y表示完全反应后试管中剩余气体的体积(mL)。试以x为横坐标,y为纵坐标,在坐标系中表示出x与y的曲线关系。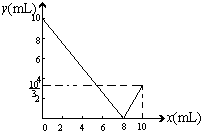
为了除去工业废气中的SO2,将“SO2转化为(NH4)2SO4”的资料摘录如下:“一个典型的实例:初步处理后的废气中含0.2%的SO2和10%O2(体积比,下同)。400℃时将废气以5m3/h的速率通过V2O5催化剂层与20L/h的速率的氨气混合,再喷入水(290g/h),此时气体温度由400℃降为200℃。在热的结晶装置中可得到(NH4)2SO4晶体(气体体积均折算成标准状况)。”利用上述资料,用氨来除去工业废气中的SO2,回答下列问题:
(1)按反应中的理论值,SO2和O2的物质的量之比是2:1,该资料中的比值是
,简述不采用2:1的理由是。
(2)通过计算,说明为什么废气以5m3/h的速率与20L/h的速率的氨气混合?
(3)若某厂每天排放1104m3这种废气,按上述方法该厂每月(按30天计算)可得硫酸铵多少吨?消耗氨气多少吨?