硼镁泥是一种工业废料,主要成份是MgO(占40%),还有CaO、MnO、Fe2O3、FeO、Al2O3、SiO2等杂质,以此为原料制取的硫酸镁,可用于印染、造纸、医药等工业。从硼镁泥中提取MgSO4·7H2O的流程如下: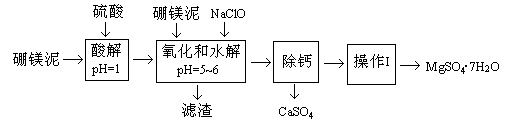
根据题意回答下列问题:
(1)实验中需用1mol/L的硫酸80mL,若用98%的浓硫酸来配制,除量筒、玻璃棒外,还需要的玻璃仪器有 。
(2)滤渣的主要成份除含有Fe(OH)3、Al(OH)3、MnO2外,还有 。
(3)加入的NaClO可与Mn2+反应产生MnO2沉淀,该反应的离子方程式 。在调节pH=5-6之前,还有一种离子也会被NaClO氧化,该反应的离子方程式为 。
(4)如何检验滤液中Fe3+是否被除尽,简述检验方法 。
(5)已知MgSO4、CaSO4的溶解度如下表:
| 温度(℃) |
40 |
50 |
60 |
70 |
| MgSO4 |
30.9 |
33.4 |
35.6 |
36.9 |
| CaSO4 |
0.210 |
0.207 |
0.201 |
0.193 |
“除钙”是将MgSO4和CaSO4混合溶液中的CaSO4除去,根据上表数据,简要说明操作步骤 、 。
(6)如果提供的硼镁泥共100 g,得到的MgSO4·7H2O 196.8 g,则MgSO4·7H2O的产率为 。
已知15.6gNa2X固体中含有0.4molNa+。
(1)X的相对原子质量为,如果X原子中质子数和中子数相等,则X是元素(填元素名称)。
(2)将39gNa2X固体溶解到水中,并加水稀释至2L。此时溶液中Na+的物质的量浓度为,从中取出100mL溶液,此时溶液中Na+的物质的量浓度为,则其中所含Na+的数目是。
欲除去下列物质中所含的杂质(括号内为杂质),请选择适当的试剂,并写出相应的化学方程式。
化学是一门以实验为基础的自然科学,化学实验在化学学习中具有重要的作用。
下列关于实验的叙述中正确的有。
| A.不慎碰翻燃着的酒精灯失火,应立即用湿布灭火 |
| B.不慎将酸沾到皮肤或衣物上,应立即用浓NaOH清洗 |
| C.用托盘天平称量物品质量时,物品应置于右盘 |
| D.实验时应节约药品,实验剩余的药品应放回原试剂瓶 |
E. 可燃性气体点燃前一定要验纯
F. 使用分液漏斗前须检查其是否漏水
将煤焦油中的苯、甲苯、苯酚进行分离,可采取如下图所示的操作方法:
(1)写出①、⑤化学式:、
(2)写出分离方法②和③的名称:、
(3)下层液体④通入气体⑤反应的离子方程式:。
维生素A是一切健康上皮组织必需的物质,缺乏维生素A时会引起儿童发育不良,导致干眼病、夜盲症、皮肤干燥等多种病症。右图是维生素A的结构。
请回答:
(1)维生素A的分子式为
(2)下列物质在一定条件下能与维生素A反应的是(填标号)
| A.溴水 | B.酸性高锰酸钾溶液 | C.乙酸 | D.新制CuO E.NaOH溶液 |
(3)如果有机物分子中所含氢原子个数比其同碳原子数少的“烷”少,称为“缺氢指数”或“不饱和度”,如 和环丙烷的不饱和度为1,
和环丙烷的不饱和度为1,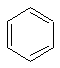 和
和 的不饱和度为4。由此推断,维生素A的不饱和度为
的不饱和度为4。由此推断,维生素A的不饱和度为