下列有关电解质溶液中微粒的物质的量浓度关系错误的是( )
| A.在0.1 mol·L-1NaHCO3溶液中:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) |
| B.在0.1 mol·L-1Na2CO3溶液中:c(OH-)-c(H+)=c(HCO3-)+2c(H2CO3) |
| C.向0.2 mol·L-1NaHCO3溶液中加入等体积0.1 mol·L-1NaOH溶液: c(HCO3-) > c(CO32-)> c(OH-)>c(H+) |
| D.常温下,CH3COONa和CH3COOH混合溶液[pH=7, c(Na+)=0.1 mol·L-1]:c(Na+)=c(CH3COO-)>c(H+)=c(OH-) |
根据化学反应方程式:I2+SO2+2H2O=H2SO4+2HI、2FeCl2+Cl2=2FeCl3、2FeCl3+2HI=2FeCl2+2HCl+I2,判断有关物质的还原性顺序正确的是
A.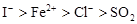 |
B.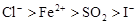 |
C.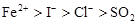 |
D.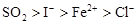 |
实验室做铜和浓硫酸的反应实验时,玻璃导管口可缠放一团蘸有Na2CO3溶液的棉花,目的是
| A.检验反应产生的气体 | B.除去产生的杂质气体 |
| C.使气体冷凝回流 | D.防止产生的气体污染空气 |
下列对硫酸的叙述正确的是
| A.浓硫酸具有强氧化性,故不可用它来干燥还原性气体二氧化硫 |
| B.浓硫酸不活泼,可用铁铝容器存放 |
| C.浓硫酸有强氧化性,稀硫酸没有氧化性 |
| D.浓硫酸难挥发,可用来制HF、HCl等挥发性酸 |
盛有氯化钡稀溶液的甲乙两试管分别通入SO2至饱和,若向甲试管中加入足量氯水,乙试管中加入足量氢氧化钠溶液,则下列叙述正确的是
| A.甲、乙两试管都有白色沉淀生成 |
| B.甲、乙两管都没有白色沉淀生成 |
| C.甲管没有白色沉淀生成而乙试管有 |
| D.甲管有白色沉淀而乙试管没有 |
下列物质均有漂白作用,但其中一种的漂白原理与其他三种不同的是
| A.HClO | B.SO2 | C.O3 | D.木炭 |