(14分)回答下列关于铁元素及其化合物的知识:
(1)向一支装有FeCl3溶液的试管中滴加NaOH溶液,现象为 _________________,
其中含铁元素的产物的化学式是___________________ ;
(2)为了检验某未知溶液是否含有Fe2+离子,两位同学分别设计了以下实验方案加以证明。方案一:向一支装有该未知溶液的试管中先通入氯气,再滴加KSCN溶液,溶液呈现红色,证明该未知溶液含有Fe2+离子;
方案二:向另一支装有该未知溶液的试管中先滴加KSCN溶液,无现象,再通入氯气,溶液变为红色,证明该未知溶液含有Fe2+离子;
则请回答:①你认为哪个方案较为合理 __________________ ;
②写出Fe2+与氯气反应的离子方程式 ____________________________;
③实验室在保存含有Fe2+离子的溶液时,为了防止Fe2+离子变质,经常向其中加入铁粉,
其原因是(用离子方程式表示)__________________________________________
(4)鲜榨苹果汁是人们喜爱的饮料。由于此饮料中含有Fe2+,鲜榨的苹果汁在空气中会由淡绿色的Fe2+变为棕黄色的Fe3+,则这个变色的过程中Fe2+被______ ;若在榨汁的时候加入适量的维生素C,可有效防止这种现象的发生。这说明维生素C具有_______。
| A.氧化性 | B.还原性 | C.酸性 | D.碱性 |
拆开1 mol H—H键,1 mol N—H键,1 mol N≡N键分别需要吸收的能量为436 kJ,391 kJ,946 kJ。则1 mol N2生成NH3_1____热量(填“吸收”或“放出”) _2__kJ;理论上,每生成1 mol NH3__3_热量(填“吸收”或“放出”) 4kJ;事实上,反应的热量总小于理论值,为什么?_________5_________________。
下列反应属于放热反应的是 1;属于吸热反应的是 2。
| A.锌粒与稀H2SO4反应制取H2 | B.氢气在氧气中燃烧 |
| C.碳酸钙高温分解成氧化钙和二氧化碳 | D.氢氧化钾和硫酸中和 |
E.Ba(OH)2·8H2O与NH4Cl反应F.氢气还原氧化铜
G.葡萄糖在人体内氧化分解 H.钢铁制品生锈的反应
用电子式表示下列物质的形成过程:(4分)
NaF:
②H2S:
写出下列物质的电子式
H2O 1KOH 2
CO2: 3Na2O2: 4
由短周期元素组成的单质A、B、C和甲、乙、丙、丁四种化合物有下图所示的转化关系,已知C为密度最小的气体。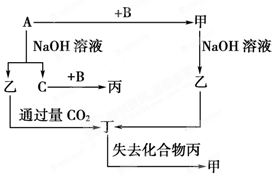
根据图示转化关系回答:
(1)写出下列物质的化学式:B、丙、丁。
(2)组成单质A的元素在周期表中的位置是。
(3)乙与过量CO2反应的离子反应方程式____________________________
(4)A与NaOH溶液反应的化学反应方程式____________________________