拆开1 mol H—H键,1 mol N—H键,1 mol N≡N键分别需要吸收的能量为436 kJ,391 kJ,946 kJ。则1 mol N2生成NH3_1____热量(填“吸收”或“放出”) _2__ kJ;理论上,每生成1 mol NH3__3_热量(填“吸收”或“放出”) 4 kJ;事实上,反应的热量总小于理论值,为什么?_________5_________________。
(9分)某有机化合物A含碳76.6%、含氢6.4%,A的相对分子质量约是甲烷的5.9倍。在常温下,该有机物的稀溶液可与浓溴水反应生成白色沉淀,1molA恰好跟3molBr2反应。
(1)求A的分子式 。
(2)写出A的稀溶液中滴加浓溴水的化学方程式__________________。
(3)写出A与碳酸钠、碳酸氢钠溶液可能发生的反应的离子方程式。
(12分)乙烯是重要的化工原料,可以合成很多有机物。以下转化关系中A-J均为有机化合物,H为有芳香气味的液体,F的分子式为C2H2O2,I分子中有一个六原子环状结构。部分反应条件和生成物已略去。完成下列问题:
(1)写出A生成B的化学方程式:。
(2)写出A生成J的化学方程式:。
(3)写出D生成E的化学方程式:________________________________________。
(4)写出E和G生成I的化学方程式:。
质谱、红外光谱、核磁共振等物理方法已成为研究有机物的重要组成部分。

(1) 下列物质中,其核磁共振氢谱中给出的峰值只有一个的是
A.CH3CH3 B.CH3COOH C.CH3COOCH3 D.CH3OCH3
(2)化合物A和B的分子式都是C2H4Br2, A的核磁共振氢谱图如右图所示,则A的结构简式为,请预测B的核磁共振氢谱上应该有个峰(信号)。
(3)化合物C中各原子数目比为:N(C):N(H):N(O)=1:2:1,对化合物C进行质谱分析可得到右图所示的质谱图,可得出其分子式为。若对其进行红外光谱分析,可得出其官能团为 (写名称)。确定化合物C的官能团时,你认为(填“有”或“没有”)必要进行红外光谱分析。写出化合物C与足量新制氢氧化铜反应的化学方程式:。
(10分)按下面步骤由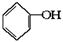 合成
合成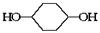 (部分试剂和反应条件已略去)。
(部分试剂和反应条件已略去)。
请回答下列问题:
(1)分别写出B、D的结构简式:B_________、D_________。
(2)反应①~⑦中属于消去反应的是。(填数字序号)
(3)如果不考虑⑥、⑦反应,对于反应⑤,得到的E可能的结构简式为:____________________。
(4)试写出C→D反应的化学方程式(注明反应条件)。
(14分)现有六种元素,其中A、B、C、D为短周期主族元素,E、F为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
| A元素原子的核外p电子总数比s电子总数少1 |
| B元素原子核外s电子总数与p电子总数相等,且不与A元素在同一周期 |
| C原子核外所有p轨道全满或半满 |
| D元素的主族序数与周期数的差为4 |
| E是前四周期中电负性最小的元素 |
| F在周期表的第七列 |
(1)A基态原子中能量最高的电子,其电子云在空间有个方向,原子轨道呈形。
(2)某同学根据上述信息,所画的B电子排布图如图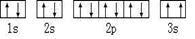 ,违背了原理。
,违背了原理。
(3)F位于族区,其基态原子有种运动状态。
(4)CD3 中心原子的杂化方式为,用价层电子对互斥理论推测其分子空间构型为,检验E元素的方法是。
(5)若某金属单质晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示。则晶胞中该原子的配位数为,该单质晶体中原子的堆积方式为四种基本堆积方式中的。若已知该金属的原子半径为d cm,NA代表阿伏加德罗常数,金属的相对原子质量为M,则该晶体的密度为______g·cm-3(用字母表示)。