下列是实验操作中,能达到实验目的是( )
| A.用100mL量筒量取5.2mL盐酸 |
| B.用托盘天平称取25.20g氯化钠 |
| C.用100mL容量瓶配制50mL 0.1mol·L-1盐酸 |
| D.用25.00mL碱式滴定管量取14.80mL NaOH溶液 |
进行一氯取代后,只生成三种沸点不同的产物的烷烃是
| A.(CH3)2CHCH2CH2CH3 | B.(CH3CH2)2CHCH3 |
| C.(CH3)2CHCH(CH3)2 | D.(CH3)3CCH2CH3 |
下列有机物名称正确的是
| A.2-乙基戊烷 | B.1,2-二氯丁烷 |
| C.2,2-二甲基-4-己醇 | D.3,4-二甲基戊烷 |
下列属于分离、提纯固态有机物的操作的是
| A.蒸馏 | B.萃取 | C.重结晶 | D.分液 |
下列物质的类别与所含官能团都正确的是
A.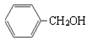 酚类 –OH 酚类 –OH |
B.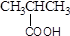 羧酸 –CHO 羧酸 –CHO |
C.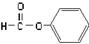 醛类 –CHO 醛类 –CHO |
D.CH3-O-CH3醚类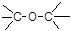 |
下列有关同系物的说法不正确的是
| A.分子组成相差一个或若干个CH2原子团的化合物必定互为同系物 |
| B.具有相同通式的有机物不一定互为同系物 |
| C.两个相邻同系物的相对分子质量数值一定相差14 |
| D.分子式为C3H8与C6H14的两种有机物一定互为同系物 |