A、B、C是中学化学中常见的三种短周期元素。已知:①A元素原子最外层电子数是次外层电子数的2倍;②B元素最高正价与最低负价的代数和为2;③C元素有多种化合价,且常温下C元素的单质与某种一元强碱溶液反应,可得到两种含C元素的化合物;④B、C两种元素质子数之和是A元素质子数的4倍。
(1)写出常温下C的单质和强碱溶液反应的离子方程式____________________。
(2)意大利罗马大学的FuNvio Cacace等人获得了极具理论研究意义的B4气态分子。B4分子结构与白磷分子结构相似 ,已知断裂1 mol B—B键吸收167 kJ的热量,生成1 mol B≡B键放出942 kJ热量。试判断相同条件下B4与B2的稳定性顺序是:______________。
,已知断裂1 mol B—B键吸收167 kJ的热量,生成1 mol B≡B键放出942 kJ热量。试判断相同条件下B4与B2的稳定性顺序是:______________。
 (3)由B、C两种元素组成的化合物X,常温下为易挥发的淡黄色液体,X分子为三角锥形分子,且分子里B、C两种原子最外层均达到8个电子的稳定结构。X遇水蒸气可形成一种常见的漂白性物质。则X与水反应的化学方程式是____________________________。
(3)由B、C两种元素组成的化合物X,常温下为易挥发的淡黄色液体,X分子为三角锥形分子,且分子里B、C两种原子最外层均达到8个电子的稳定结构。X遇水蒸气可形成一种常见的漂白性物质。则X与水反应的化学方程式是____________________________。
(4)A、B两种元素可形成一种硬度比金刚石还大的化合物Y。在化合物Y中,A、B原子间以单键相结合,且每个原子的最外层均达到8个电子的稳定结构。则Y的化学式为
______________,其熔沸点比金刚石_____(填“高”、“低“或“无法比较”)。
已知:用惰性电极电解某盐X的溶液,发生的反应为:
X+H2O  A(单质)+B(单质)+Y(化合物)
A(单质)+B(单质)+Y(化合物)
(1)若组成X的元素均为短周期元素,且A、B均为气体,其在相同条件下体积 比为1:1,产物之间可以发生如图的反应(变化中的水略去)。写出有关反应的离子反应方程式:①_______________________________。
(2)若A为红色固体,A可以与Y的浓溶液反应生成一种与A的摩尔质量相同的气体。
①写出该电解过程中阳极的电极反应式:___________________;
②某学生电解一定浓度的X溶液一段时间后,向所得溶液中加入0.1molACO3后,恢复到电解前的浓度和pH(不考虑CO2溶解),则电解过程中转移的电子数为_______。
(3)若向X的溶液中加入过量的稀盐酸,产生白色沉淀,且存在如下的转化关系:
Ⅰ. A+Y(浓)→X+C(气体)+H2O;Ⅱ. A+Y(稀)→X+D(气体)+H2O;Ⅲ. M+O2→D(气体)+H2O。
①已知:组成M气体的两种元素质量比为14:3,则检验M的方法是___________________;
②在标准状况下,27gA溶于一定浓度的Y溶液时,产生2.8L气体,将装有该气体的量筒倒立于有水的水槽中,再通入_______L气体B,水才能恰好充满量筒。
为了测定草酸晶体(H2C2O4·xH2O)中的x值,进行如下实验
(1)称取Wg草酸晶体,配成100.00mL溶液
(2)取25.00mL所配溶液于锥形瓶内,加入适量稀H2SO4后,用浓度为amol/L的KMnO4溶液滴定至KMnO4不再褪色为止,所发生的反应为: 2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O。
试回答:
①实验中,需要的仪器有(填序号),还缺少的仪器有(填名称)
A托盘天平(带砝码、镊子) B滴定管 C 100mL的量筒 D、100mL的容量瓶
E、烧杯 F、漏斗 G、锥形瓶 H、玻璃棒 I、药匙 J、烧瓶
②实验中,标准KMnO4溶液应装在式滴定管中,因为
③若在接近滴定终点时,用少量蒸馏水将锥形瓶内壁冲洗一下,再继续滴至终点,则所测得的x的值会(填偏大、偏小、无影响)。
④在滴定过程中若用去amol/L的KMnO4溶液VmL,则所配制的草酸溶液的物质的量浓度为mol/L,由此,x=。
⑤若滴定终点读数时俯视刻度,则计算的x值会(填偏大、偏小、无影响)。
(1)蕴藏在海底的“可燃冰”是高压下形成的外观像冰的甲烷水合物固体(分子式为CH4·9H2O),则356g“可燃冰”释放出的甲烷燃烧,生成液态水时能放出1780.6 kJ的热量,则甲烷燃烧的热化学方程式可表示为:_______________________________。
(2) 在100℃时,将0.100mol的N2O4气体充入1 L恒容抽空的密闭容器中,隔一定时间对该容器内物质的浓度进行分析得到下表数据:
①从表中分析:该反应的平衡常数为___________;
②在上述条件下,60s内N2O4的平均反应速率为_____________;
③达平衡后下列条件的改变可使NO2浓度增大的是_________。
| A.增大容器的容积 | B.再充入一定量的N2O4 |
| C.再充入一定量的NO2 | D.再充入一定量的He |
(3)常温下①用等浓度的盐酸分别中和等体积pH=12的氨水和NaOH溶液,消耗盐酸的体积分别为V1、V2,则V1_____V2(填“>”“<”或“=”下同);
②用等浓度的盐酸分别中和等体积浓度均为0.01mol/L的氨水和NaOH溶液,消耗盐酸的体积分别为V3、V4,则V3_____V4;
③用等浓度的盐酸分别和等体积浓度均为0.01mol/L的氨水和NaOH溶液反应,最后溶液均为中性,消耗盐酸的体积分别为V5、V6,则V5_____V6。
簸箩酯是一种食用香料,是化合物甲与苯氧乙酸 -O-CH2-COOH发生酯化反应的产物。
-O-CH2-COOH发生酯化反应的产物。
(1)甲一定含有的官能团的名称是_________。
(2)5.8g甲完全燃烧可产生0.3molCO2和0.3molH2O,甲蒸气对氢气的相对密度是29,甲分子中不含甲基,且为链状结构,其结构简式是______________________。
(3)苯氧乙酸有多种类型的同分异构体,其中能与FeCl3溶液发生显色反应,且有2种一硝基取代物的同分异构体是(写出任意2种的结构简式)___________ _____________。
(4)已知: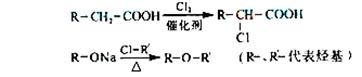
簸箩酯的合成线路如下: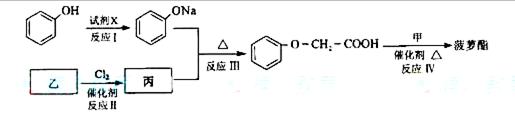
①试剂X不可选用的是(选填字母)__________。
| A.CH3COONa溶液 | B.NaOH溶液 | C.NaHCO3溶液 | D.Na |
②丙的结构简式是___________,反应Ⅱ的反应类型是_____________________。
③反应Ⅳ的化学方程式是________________。
(15分)
(1)纳米技术制成的金属燃料、非金属固体燃料、氢气等已应用到社会生活和高科技领域。单位质量的A和B单质燃烧时均放出大量热,可用作燃料。已知A和B为短周期元素,其原子的第一至第四电离能如下表所示:
| 电离能(kJ/mol) |
I1 |
I2 |
I3 |
I4 |
| A |
932 |
1821 |
15390 |
21771 |
| B |
738 |
1541 |
7733 |
10540 |
①某同学根据上述信息,推断B的核外电子排布如下图所示,该同学所画的电子排布图违背了,B元素位于周期表五个区域中的 _______区。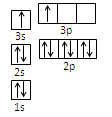
②ACl2分子中A的杂化类型为,ACl2的空间构型为。
(2)Fe原子或离子外围有较多能量相近的空轨道能与一些分子或离子形成配合物。
①与Fe原子或离子形成配合物的分子或离子应具备的结构特征是。
②六氰合亚铁离子[Fe(CN)6]4—中不存在。
A共价键 B非极性键 C配位键D.σ键 E.π键
③写出一种与 CN—互为等电子体的单质分子式。
(3)一种Al-Fe合金的立体晶胞如下图所示。请据此回答下列问题:
①确定该合金的化学式。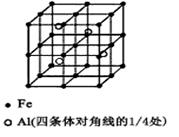
②若晶体的密度=ρg/cm3,则此合金中最近的两个Fe原子之间的距离(用含ρ的代数式表示,不必化简)为cm。