以下是对某水溶液进行离子检验的方法和结论,其中正确的是( )
A.先加入BaCl2溶液,再加入足量的HNO3溶液,产生了白色沉淀。溶液中一定含有大量的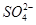 |
B.加入足量的CaCl2溶液,产生了白色沉淀。溶液中一定含有大量的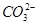 |
C.加入足量浓 NaOH溶液,产生了带有强烈刺激性气味的气体。溶液中一定含有大量的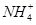 |
| D.先加适量的盐酸将溶液酸化,再加AgNO3溶液,产生了白色沉淀。溶液中一定含有大量的Cl- |
有关杂化轨道理论的说法不正确的是
| A.杂化前后的轨道数不变,但轨道的形状发生了改变 |
| B.sp3、sp2、sp杂化轨道的夹角分别为109°28′、120°、180° |
| C.四面体形、三角锥形的结构可以用sp3杂化轨道解释 |
| D.杂化轨道全部参加形成化学键 |
若某原子在处于能量最低状态时,外围电子排布为3d14s2,则下列说法正确的是
| A.该元素原子处于能量最低状态时,原子中共有3个未成对电子 |
| B.该元素原子核外共有4个能层 |
| C.该元素原子的M能层共有8个电子 |
| D.该元素原子最外层共有3个电子 |
有关核外电子运动规律的描述错误的是
| A.核外电子质量很小,在原子核外作高速运动 |
| B.核外电子的运动规律与普通物体不同,不能用牛顿运动定律来解释 |
| C.在电子云示意图中,通常用小黑点来表示电子绕核作高速圆周运动 |
| D.在电子云示意图中,小黑点密表示电子在核外空间单位体积内电子出现的机会多 |
下列电子排布式中,原子处于激发态的是
| A.1s22s22p1 | B.1s22s22p33s1 |
| C.1s22s22p63s23p63d104s2 | D.1s22s22p63s23p63d34s2 |
现有5种基团:—CH3、—OH、—CHO、—COOH、—C6H5,对由其中两两基团构成且显酸性的有关物质叙述正确的是
| A.共有4种,其中一种物质不属于羧酸 |
| B.共有5种,其中一种为二元酸 |
| C.共有6种,其中只有一种不是有机酸 |
| D.共有6种,它们在一定条件下均能与乙醇发生酯化反应 |