性质决定用途,化学知识运用得当可以使人类的生活更美好。下列物质性质与应用的对应关系正确的是
| A.晶体硅熔点高硬度大,可用于制作半导体材料 |
| B.浓硫酸具有酸性,可用于刻蚀玻璃制品 |
| C.漂白粉在空气中不稳定,可用于漂白纸张 |
| D.氢氧化铝具有弱碱性,可用于制胃酸中和剂 |
下列说法错误的是()
A.同系物 一定符合同一通式 一定符合同一通式 |
| B.同分异构体一定具有相同的最简式 |
| C.一种元素形成不同的物质可能互为同分异构体 |
| D.同系物的化学性质相似,物理性质随着碳原子数增加而有规律的变化 |
某烃的一种同分异构体只能生成一种一氯代物,该烃的分子式是()
| A.C3H8 | B.C4H10 |
| C.C5H12 | D.C6H14 |
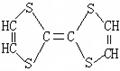
用于制造隐形飞机的某种物质具有吸收微波的功能,其主要成分的结构如图,它属于
()
| A.无机物 | B.烃 |
| C.高分子化合物 | D.有机物 |
可逆反应2NO2 2NO+O2在体积不变的密闭容器中反应,达到平衡状态的标志是()
2NO+O2在体积不变的密闭容器中反应,达到平衡状态的标志是()
①单位时间内生成n molO2的同时生成2n mol NO2
②单位时间内生成n molO2的同时生成2n mol NO
③用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2 : 2 : 1的状态
④混合气体的颜色不再改变的状态
⑤混合气体的密度不再改变的状态
⑥混合气体的平均相对分子质量不再改变的状态
| A.①④⑥ | B.②③⑤ | C.①③④ | D.①②③④⑤ |
短周期中元素a、b、c在周期表中位置如右图,下列有关这三种元素的叙述正确()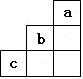
| A.a是一种活泼的非金属元素 |
| B.c的最高价氧化物的水化物是一种弱酸 |
| C.b的氢化物很稳定 |
D. b元素在化合物中的最高价为+7价 b元素在化合物中的最高价为+7价 |