在生活、生产及化学研究中,人们经常需要根据不同原子、分子或离子的某些特征应对物质进行检验,以确定物质的组成。下列有关物质检验的说法正确的是( )
| A.MnO2、CuO、Fe三种物质的粉末都是黑色的,用稀盐酸不能将它们区别开 |
| B.(NH4)2SO4、K2SO4、NH4C1三种物质不能用一种试剂通过化学反应区别开 |
| C.可以用焰色反应来检验氯化钾固体和氯化钠固体 |
| D.用湿润的KI淀粉试纸可以检验溴蒸气中是否含有氯气 |
下列叙述中正确的是
| A.H2SO4的摩尔质量是98 |
| B.CO的摩尔质量为28 g/ mol |
| C.1 molO的质量是16g/ mol |
| D.将98gH2SO4溶解于500 mL水中,所得溶液中H2SO4的物质的量浓度为2 mol/L |
一化学兴趣小组在家中进行化学实验,按照图1连接好线路发现灯泡不亮,按照图2连接好线路发现灯泡亮,由此得出的结论正确的是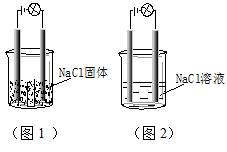
| A.NaCl是非电解质 |
| B.NaCl溶液是电解质 |
C.N aCl在水溶液中电离出了可以自由移动的离子 aCl在水溶液中电离出了可以自由移动的离子 |
| D.NaCl溶液中水电离出大量的离子 |
下列叙述中正确的是
| A.氧化还原反应中氧化剂得电子,化合价升高 |
| B.氧化还原反应中,一种物质被氧化,另一种物质必然被还原 |
| C.氧化还原反应的实质是电子的转移(得失或偏移) |
| D.物质所含元素化合价升高的反应是还原反应 |
下列实验方案可行的是
| A.用澄清石灰水检验CO2含有的CO |
| B.用经盐酸酸化的AgNO3溶液检验溶液中含有的Cl- |
| C.用蒸馏水鉴别无水硫酸铜、碳酸钙、氯化铵 |
| D.用溶解、过滤的方法分离 CaCl2 和NaCl固体混合物 |
水是一种重要的化学试剂。分析下列反应,水只作还原剂的是
A.2 H2O 2 H2↑+ O2↑ 2 H2↑+ O2↑ |
B.2Na + 2 H2O="2" NaOH + H2↑ |
| C.2 F2 + 2 H2O=" 4" HF + O2 | D.CO2 + H2O = H2CO3 |