化学兴趣小组同学运用类比学习的思想,探究过氧化钠与二氧化硫的反应。小组同学改进了下图所示的装置进行实验制取SO2的反应。充分反应,B中固体由淡黄色变为白色(Na2O2完全反应),将带火星的木条插入试管C中,木条复燃。试回答下列问题:
(1)请你完成装置改进的措施和理由:
①措施:在A、B之间加一个干燥管,作用_______________________________________。
②措施:为确保C中的实验现象发生,在B、C之间加一个装有_________________的洗气瓶,作用_______________________。
(2)某同学推断该白色固体为Na2SO3,则其化学反应方程式是__________________。
(3)任何的推论都要经过检验,请完成对白色固体成分的探究:
限选实验仪器与试剂:烧杯、试管、药匙、滴管、酒精灯、带单孔胶塞的导管、棉花、试管夹;3 mol·L-1HCl、6 mol·L-1HNO3、NaOH稀溶液、蒸馏水、1 mol·L-1 BaCl2溶液、澄清石灰水、品红溶液。
①提出合理假设:
假设1:白色固体为Na2SO3; 假设2: ;
假设3:白色固体为Na2SO3与Na2SO4的混合物。
②设计实验方案证明以上三种假设,并按下表格式写出实验操作步骤、预期现象与结论。
| 实验操作 |
预期现象与结论 |
| 步骤1:取少量白色固体于试管,加入 ,塞上单孔胶塞,将生成的气体通入 。 |
若 ,说明白色固体含有Na2SO3,则 成立,若无该现象, 则 成立。 |
| 步骤2:在步骤1反应后的溶液加入 。 |
若 ,则说明白色固体含Na2SO4。 结合步骤1的结论,则 成立,若无该现象,则 则 成立。 |
虚线框中的装置可用来检验浓硫酸与木炭粉在加热条件下反应所产生的所有气体产物。请填写下列空白。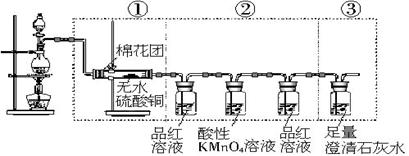
(1)如果将图示装置中①、②、③三部分仪器的连接顺序变为②、①、③,则可检验出来的物质是_____;不能检验出来的物质是______。
(2)如果将仪器的连接顺序变为①、③、②,则可检验出来的物质是_____;不能检验出来的物质是_______。
(3)如果将仪器的连接顺序变为②、③、①,则可检验出来的物质是______;不能检验出来的物质是________
某学习小组探究浓、稀硝酸氧化性的相对强弱,按下图装置进行实验(夹持仪器已略去)。实验表明浓硝酸能将NO氧化成NO2,而稀硝酸不能氧化NO。由此得出的结论是浓硝酸的氧化性强于稀硝酸。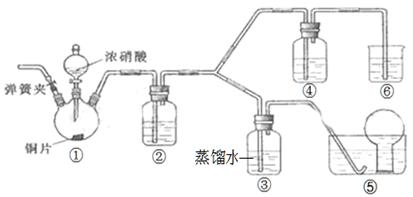
可选药品:浓硝酸、3mo/L稀硝酸、蒸馏水、浓硫酸、氢氧化钠溶液及CO2。
已知氢氧化钠溶液不与NO反应,能与NO2反应:2NO2+2NaOH=NaNO3+NaNO2+H2O。
(1)实验应避免有害气体排放到空气中,装置③、④、⑥中盛放的药品依次是、
、。
(2)滴加浓硝酸之前,需打开弹簧夹,通入一段时间的CO2,其目的是
。
(3)装置①中发生反应的离子方程式是。
(4)装置②的作用是,发生反应的化学方程式是。
(5)该小组得出的结论依据的实验现象是。
(6)实验结束后,同学们发现装置①中溶液呈绿色,而不显蓝色。甲同学认为是该溶液中硝酸铜的质量分数较高所致,而乙同学认为是该溶液中溶解了生成的气体。同学们分别设计了以下4个试验来判断两种看法是否正确。这些方案中可行的是。(可多选)
a.加热该绿色溶液,观察颜色变化
b.加水稀释绿色溶液,观察颜色变化
c.向该绿色溶液中通入氧气,观察颜色变化
d.向饱和硝酸铜溶液中通入浓硝酸与铜反应产生的气体,观察颜色变化
某化学兴趣小组为探究SO2的性质,查阅相关资料知:实验室制取SO2气体的反应原理为Na2SO3 + H2SO4  Na2SO4 + SO2↑+ H2O,据此设计如下图所示装置进行相关实验。
Na2SO4 + SO2↑+ H2O,据此设计如下图所示装置进行相关实验。
|
指出下面3个实验中各存在的一个错误:
A___________________ B_____________________ C__________________
三草酸合铁酸钾晶体(K3[Fe(C2O4)3]·xH2O)是一种光敏材料,在110℃可完全失去结晶水。为测定该晶体中铁的含量,某实验小组做了如下实验:
步骤一:称量5.40g三草酸合铁酸钾晶体,配制成250ml溶液。
步骤二:取所配溶液25.00ml于锥形瓶中,加稀H2SO4酸化,滴加KMnO4溶液至草酸根恰好全部氧化成二氧化碳,同时,MnO4-被还原成Mn2+。向反应后的溶液中加入适量锌粉使Fe3+全部转化为Fe2+,同时有气泡产生,过滤,洗涤,将过滤及洗涤所得溶液A收集到锥形瓶中,此时,溶液仍呈酸性。
步骤三:用0.010mol/L KMnO4溶液滴定溶液A至终点,消耗KMnO4溶液21.98ml,反应中MnO4-被还原成Mn2+ 。
重复步骤二、步骤三操作,消耗0.010mol/L KMnO4溶液22.02ml。
请回答下列问题:
①配制三草酸合铁酸钾溶液的操作依次是:称量、溶解、冷却、转移、洗涤、、摇匀。
②“步骤一”所得溶液的颜色为。
③写出“步骤二”中加锌粉产生气泡的离子方程式;
写出“步骤二”中Fe3+转化为Fe2+的离子方程式。
④“步骤三”KMnO4溶液应装在式滴定管中;检查该滴定管不漏水,用水洗净后,装入KMnO4标准溶液前,要对该滴定管进行的操作是 ;
判断滴定至终点依据的现象是 。
⑤实验测得该晶体中铁的质量分数为。