化合物IV为一种重要化工中间体,其合成方法如下: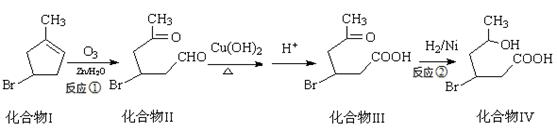
(1)化合物I的化学式为 。
(2)化合物Ⅱ具有卤代烃的性质,在一定条件下能生成烯,该反应条件是 。
(3)1mol化合物III与足量NaOH反应消耗NaOH的物质的量为 mol。
(4)化合物IV能发生酯化反应生成六元环化合物V,写出该反应的化学方程式
。
(5) 异黄樟油素( 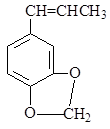 )发生类似反应①的反应,得到一种环状化合物Ⅵ(一种香料),化合物Ⅵ的结构简式为______________________。
)发生类似反应①的反应,得到一种环状化合物Ⅵ(一种香料),化合物Ⅵ的结构简式为______________________。
根据下列化合物:
①NaCl;②NaOH;③HCl;④NH4Cl;⑤CH3COONa;⑥CH3COOH;⑦NH3·H2O;⑧H2O
回答下列问题。
(1)NH4Cl溶液显性,用离子方程式表示原因,其溶液中离子浓度大小顺序为。
(2)常温下,pH=11的CH3COONa溶液中,水电离出来的c(OH-)=,在pH=3的CH3COOH溶液中,水电离出来的c(H+)=。
(3)已知纯水中存在如下平衡:H2O+H2O H3O++OH- ΔH>0,现欲使平衡向右移动,且所得溶液显酸性,可选择的方法是(填字母序号)。
H3O++OH- ΔH>0,现欲使平衡向右移动,且所得溶液显酸性,可选择的方法是(填字母序号)。
| A.向水中加入NaHSO4固体 |
| B.向水中加Na2CO3固体 |
| C.加热至100 ℃[其中c(H+)=1×10-6 mol·L-1] |
| D.向水中加入(NH4)2SO4固体 |
(4)若将等pH、等体积的②NaOH溶液和⑦NH3·H2O溶液分别加水稀释m倍、n倍,稀释后两种溶液的pH仍相等,则m(填“<”、“>”或“=”)n。
(5)除⑧H2O外,若其余7种物质的溶液的物质的量浓度相同,则这7种物质的溶液按pH由大到小的顺序为。
物质A~E都是由下表中的离子组成的,常温下将各物质的溶
液从1 mL稀释到1 000 mL,pH的变化关系如图甲所示,其中A与D反应得到E。请回答下列问题。
| 阳离子 |
NH4+、H+、Na+ |
| 阴离子 |
OH-、CH3COO-、Cl- |

(1)根据pH的变化关系,写出物质的化学式:B,C。
(2)写出A与C反应的离子方程式:。
(3)图乙为室温时向25 mL某浓度的B溶液中逐滴滴加0.2 mol·L-1的D溶液的过程中pH的变化曲线。
①图乙中B的物质的量浓度为mol·L-1。
②G点溶液呈中性,则二者恰好完全反应的点是在FG区间还是GH区间?区间。
③FG区间溶液中各离子浓度大小关系是。
(4)t ℃时,A的稀溶液中c(H+)=10-a mol·L-1,c(OH-)=10-b mol·L-1,已知a+b=13,该温度下(t ℃),将100 mL 0.2 mol·L-1的C溶液与100 mL 0.4 mol·L-1的B溶液混合后(溶液体积变化忽略不计),溶液的pH=。
已知:常温下,A酸的溶液pH=a,B碱的溶液pH=b。
(1)若A为盐酸,B为氢氧化钡,且a=3,b=11,两者等体积混合,溶液的pH为。
a.大于7 b.等于7 c.小于7
(2)若A为醋酸,B为氢氧化钠,且a=4,b=12,那么A溶液中水电离出的氢离子浓度为mol/L,B溶液中水电离出的氢离子浓度为mol/L。
(3)若A的化学式为HR,B的化学式为MOH,且a+b=14,两者等体积混合后溶液显碱性。则混合溶液中必定有一种离子能发生水解,该水解反应的离子方程式为。
中学化学实验中,淡黄色的pH试纸常用于测定溶液的酸碱性。在25 ℃时,若溶液的pH=7,试纸不变色;若pH<7,试纸变红色;若pH>7,试纸变蓝色。而要精确测定溶液的pH,需用pH计。pH计主要通过测定溶液中H+浓度来测定溶液的pH。
(1)已知水中存在平衡:H2O H++OH- ΔH>0,现欲使平衡向右移动,且所得溶液呈酸性,选择的方法是(填字母)。
H++OH- ΔH>0,现欲使平衡向右移动,且所得溶液呈酸性,选择的方法是(填字母)。
| A.向水中加入NaHSO4 |
| B.向水中加入Cu(NO3)2 |
| C.加热水至100 ℃[其中c(H+)=1×10-6 mol·L-1] |
| D.在水中加入(NH4)2SO4 |
(2)现欲测定100 ℃沸水的pH及酸碱性,若用pH试纸测定,则试纸显色,溶液呈性(填“酸”、“碱”或“中”);若用pH计测定,则pH7(填“>”、“<”或“=”),溶液呈性(填“酸”、“碱”或“中”)。
炼金废水中含有络离子[Au(CN)2]-,其电离出的CN-有毒,当CN-与H+结合生成HCN时,毒性更强。回答下列问题。
(1)剧毒物HCN的水溶液酸性很弱,写出其电离的方程式:。
(2)与弱电解质碳酸的电离方式相似,[Au(CN)2]-也存在着两步电离,其一级电离方程式为。
(3)处理这种废水是在碱性条件下,利用NaClO将CN-氧化为CO32-和N2,其离子方程式为。在酸性条件下,ClO-也能氧化CN-,但实际处理废水时却不在酸性条件下进行的主要原因是。