已知某浓度的硫酸在水中的电离方程式:
H2SO4=H++HSO4-,HSO4- H++ SO42-。
H++ SO42-。
(1)Na2SO4溶液显__________(填“酸性”“碱性”或“中性”),理由是(用离子方程式表示)_________。
(2)在25 ℃时0.1 mol·L-1的NaHSO4溶液中c(SO42-)="0.029" mol ·L-1,则25 ℃时,0.1 mol·L-1 H2SO4溶液中c(SO42-)_________0.029 mol ·L-1(填“大于”,“小于”或“等于”),理由是 。
(3)在0.1 mol ·L-1 Na2SO4溶液中,下列粒子浓度关系正确的是 。
| A.c(Na+)+c(H+)=c(OH-)+c(HSO4-)+2c(SO42-) |
| B.2c(Na+)=c(SO42-)+c(HSO4-) |
| C.c(Na+)>c(SO42-)>c(H+)>c(OH-) |
| D.c(SO42-)+c(HSO4-)=0.1 mol·L-1 |
下图1是工业上“碱法烟气脱硫法” 示意图,下图2是工业上“石灰→石膏烟气脱硫法”示意图,回答: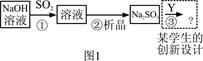

已知:
| 试剂 |
Ca(OH)2 |
NaOH |
| 价格(元/kg) |
0.36 |
2.9 |
| 吸收SO2的成本(元/mol) |
0.027 |
0.232 |
(1)图1中,反应①的离子方程式为,之一是。
(2)图2中,反应⑤的目的是稳定固化硫元素形成高价态的化合物,氧气的作用是。该法的优点之一是。
(3)“碱法烟气脱硫法”中的产物Na2SO3的稳定性不好,易使硫元素重新转化为挥发性污染物,为避免之,设计了③的反应,写出其化学方程式为。
实验室需用90mL 2mol·L-碳酸钠溶液。
(1)配制该溶液时,根据你的实践经验,下列仪器不可能用到的是_____(填选项)。
A. 托盘天平 B. 烧杯 C. 胶头滴管 D. 100ml容量瓶 E. 90ml容量瓶 F.玻璃棒
(2)实验操作步骤有:A.称取碳酸钠晶体;B.用少量的水将烧杯等仪器洗涤2~3次,每次洗涤液也转移到容量瓶;C.将烧杯中的溶液转移到选定的容量瓶中;D.将碳酸钠晶体置于烧杯中用适量的水溶解,并用玻璃棒搅拌均匀;E.将配好的碳酸钠溶液装入试剂瓶待用并贴好标签;F.向容量瓶加水至刻度线1-2cm处改用胶头滴管滴加水至液面与刻度线相切;G.塞好瓶塞,反复上下颠倒摇匀。
①上述步骤的正确操作顺序是B(填写字母)
②本实验称取的碳酸钠晶体的质量是g
③若定容时仰视刻度线,则所配溶液浓度(填“偏大”、“偏小”或“无影响”)
④用胶头滴管往容量瓶中加水时,不小心液面超过了刻度,处理方法是(填选项)。
A. 吸出多余液体,使凹液面与刻度线相切
B. 小心加热容量瓶溶液,经蒸发后,使凹液面与刻度线相切
C. 经准确计算加入一定量的浓硫酸
D. 重新配制碳酸钠溶液
下图①—⑩分别代表有关反应中的一种物质,其中③气体能使酚酞试液变红,⑦是红综色气体,回答: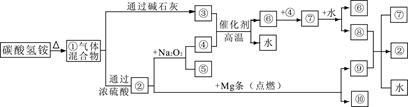
(1)①中的混合气体通过浓硫酸发生化学反应,主要生成物的化学式是。
(2)写出碳酸氢铵中阳离子的检验方法。
(3)写出工业上合成③的化学方程式。
(4)⑧与⑨反应的化学方程式是。
有一瓶无色澄清的溶液,其中可能含Na+、Mg2+、H+、Fe3+、CO32-、Cl-、Br-中的一种或几种,取该溶液进行如下实验:
①用PH试纸检验,表明溶液呈强酸性
②取部分溶液,加入少量的CCl4及数滴新制的氯水,振荡后CCl4层显橙红色
③将②得到的溶液滴加硝酸银溶液,有白色沉淀生成,滴加稀硝酸沉淀不溶解。
④另取部分溶液,逐滴加入稀NaOH溶液,使溶液从酸性逐渐转变为碱性,在滴加过程中及滴加完毕后,溶液中均无沉淀生成
根据上述实验事实确定并回答:
(1)在溶液中,肯定存在的离子有。
(2)肯定不存在的离子有。
(3)可能存在的离子有。
新制氯水中含有多种粒子,某校化学研究性学习小组的同学为探究其组成,做了如下实验,回答:
(1)往用水湿润的红纸中滴入少量新制饱和氯水,观察到现象,说明饱
和氯水中含有。
(2)在试管中加入少量的块状碳酸钙,再加入适量饱和氯水,充分反应,有少量气泡产
生,用离子方程式解释此现象。