下图1是工业上“碱法烟气脱硫法” 示意图,下图2是工业上“石灰→石膏烟气脱硫法”示意图,回答: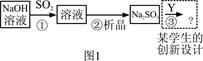

已知:
| 试 剂 |
Ca(OH)2 |
NaOH |
| 价格(元/kg) |
0.36 |
2.9 |
| 吸收SO2的成本(元/mol) |
0.027 |
0.232 |
(1)图1中,反应①的离子方程式为 ,之一是 。
(2)图2中,反应⑤的目的是稳定固化硫元素形成高价态的化合物,氧气的作用是 。该法的优点之一是 。
(3)“碱法烟气脱硫法”中的产物Na2SO3的稳定性不好,易使硫元素重新转化为挥发性污染物,为避免之,设计了③的反应,写出其化学方程式为 。
有一透明溶液,可能含有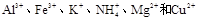 等离子中的一种或几种。现加入Na2O2粉末只有无色无味的气体放出,并同时析出白色沉淀。如加入Na2O2的量与生成白色沉淀的量之间的关系用下图来表示。
等离子中的一种或几种。现加入Na2O2粉末只有无色无味的气体放出,并同时析出白色沉淀。如加入Na2O2的量与生成白色沉淀的量之间的关系用下图来表示。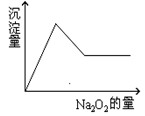
试推断:原溶液中一定含有;一定没有,可能含,为了进一步确定可能含有的离子,应增加的实验操作为,现象为。
(12分)①~⑩是元素周期表中的十种元素:
| 主族 周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
| 2 |
① |
② |
③ |
||||
| 3 |
④ |
⑤ |
⑥ |
⑦ |
⑧ |
||
| 4 |
⑨ |
⑩ |
回答下列问题:
(1)某同学对下列性质进行了对比,其中正确的是。
A.原子半径:⑩>⑨>⑦
B.离子半径:⑨>④>⑦
C.非金属性:③>②>⑥
D.单质的熔点:④>⑨>⑩>⑧
E.单质的氧化性:③>⑦>⑧
(2)用合适的化学用语回答:
金属性最强的元素离子结构示意图为,
常温下呈液态的氢化物的结构式为:。
溶于水后溶液显碱性的氢化物的电子式为:。
(3)在上述元素中,②、⑧元素形成的气态氢化物可以相互反应,该反应的化学方程式为
;⑨、⑤元素形成的最高价氧化物的水化物可以相互反应,该反应的离子方程式为。
在下列各组物质中,找出合适的序号填在对应的空格内:
①NO2和N2O4 ②12C和14C ③ 和
和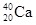
④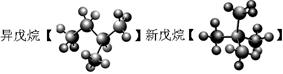
⑤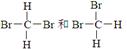
⑥甲烷与丙烷]
⑦乙醇(CH3CH2OH)和乙二醇(HO—CH2—CH2—OH)
(1)互为同位素的是 ;
(2)互为同分异构体的是 ;
(3)互为同系物的是 ;
(4)同一种物质的是 。
(每空2分,共12分) 根据下面的反应路线及所给信息填空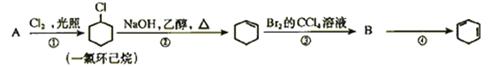
(1)A的结构简式是B的结构简式是
(2)①的反应类型是。③的反应类型是。
④的反应类型是
(3)反应④的化学方程式是。
23.(每空2分,14分)具有水果香味的中性物质A可以发生下列变化: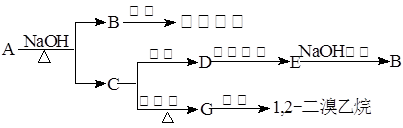
(1) 推断下述物质的结构简式:
A:________________ B:________________
C:________________ D:________________
(2) 写出下列变化的化学方程式:
A+NaOH→B+C:_____________________________________________
C→G:_________________________________________________
D→E:_________________________________________________