(14分)X、Y、Z、W均为中学化学中常见的单质或化合物,它们之间的转化关系如下图所示(水及部分产物已略去)。
(1)若X为金属单质,W是某强酸的稀溶液。X与过量W反应生成Y的离子方程式为_________。向Z溶液中加入某种试剂_______(填试剂名称或化学式),若出现蓝色沉淀,即可判断Z溶液中阳离子的存在。
(2)若X为非金属单质,W是空气的主要成分之一。它们之间转化的能量变化如图A所示,则X+W→Z的热化学方程式为_______。
(3)若X、Y为正盐,X的水溶液显酸性,W为一元强碱(化学式为MOH),Z的电离方程式为_______。室温下,若用0.1 mol/L的W溶液滴定V mL 0.1 mol/L HA溶液,滴定曲线如图B所示,则a、b、c、d四点溶液中水的电离程度最大的是______点;a点溶液中离子浓度的大小顺序为______________;取少量c点溶液于试管中,再滴加0.1 mol/L盐酸至中性,此时溶液中除H+、OH-外,离子浓度的大小顺序为______________。
(4)若X为强碱,常温下W为有刺激性气味的气态氧化物。常温时,将Z的水溶液露置于空气中,请在图C中画出其pH随时间(t)的变化趋势曲线图(不考虑水的挥发)。
(1)为鉴定硅产品中是否含有微量铁单质,将硅产品用稀盐酸溶解,取上层清液后需要加入的试剂是(填字母代号)
a.氯水b.NaOH溶液c.KSCN溶液d.Na2SO3溶液
(2)用下图装置来验证浓硫酸与木炭在加热条件下反应的产物中含有SO2和CO2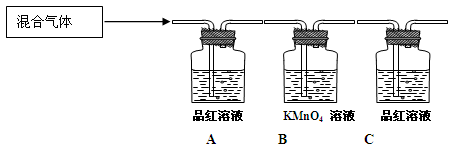
①可观察到A瓶溶液中的现象为。
②写出B瓶中的离子反应方程式为。
③C瓶溶液的作用是。
(3)取A、B两份物质的量浓度相等的NaOH溶液,体积均为50mL,分别向其中通入一定量的CO2后,再分别稀释为100mL。在稀释后的溶液中分别逐滴加入0.1mol·L-1的盐酸,产生的CO2的体积(标准状况)与所加盐酸的体积关系如图所示: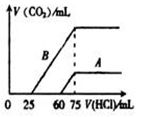
①A曲线表明,原NaOH溶液通入CO2后,所得溶液中的溶质的化学式为。
②对B曲线来说,写出横坐标上0~25 mL这一段反应的离子方程式。
按要求填写下列空白。
(1)高岭石一种硅酸盐矿物,其化学式为Al4Si4O10(OH)8,用氧化物的形式表示为。
(2)(6分,每空2分)除去下列物质中所含杂质(括号内为杂质),写出除去杂质的试剂。
①Fe2O3(Al2O3)
②SO2(HCl)
③FeCl2(FeCl3)
(3)按照题目的要求写出化学反应方程式
①两种酸混合发生反应,酸性变弱:
②两种酸混合发生反应,酸性变强:
实验研究发现,硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低。现有一定量铝粉和铁粉的混合物与一定体积某浓度的稀硝酸充分反应,反应过程中无气体放出(已知硝酸的还原产物是NH4NO3)。在反应结束后的溶液中,逐滴加入5mol·L-1的NaOH溶液,所加NaOH溶液的体积(mL)与产生的沉淀的物质的量关系如下图所示。则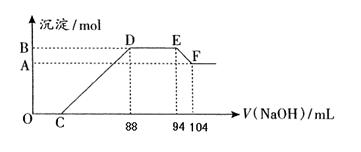
(1)B与A的差值为:mol
(2)DE段生成物的物质的量为:mol。
(3)铝粉和铁粉的混合物中铝粉与铁粉的物质的量之比为:
(4)写出铝与该浓度硝酸反应的离子方程式:
某同学欲探究Na2O2与水的反应,可供使用的试剂有:Na2O2、蒸馏水、酸性KMnO4溶液、MnO2。该同学取一定量Na2O2样品与过量水反应,待完全反应后,得到溶液X和一定量O2,该同学推测反应中可能生成了H2O2,并进行实验探究。
(1)写出Na2O2与水反应的化学方程式 。
(2)试设计实验证明溶液X中含过氧化氢 。
(3)通过上述实验证明溶液中确实存在H2O2。 取少量X于试管中,滴加FeCl2溶液,立即生成红褐色沉淀,配平下列反应的离子方程式: H2O2 + Fe2+ + OH-— Fe(OH)3¯,该反应中H2O2 表现了 性(填“氧化”或“还原”)
(4)已知溶液X可使酸性KMnO4溶液褪色,已知高锰酸钾产物为Mn2+,此时H2O2表现了 性(填“氧化”或“还原”)。该反应的离子方程式为
(1)向FeCl3溶液中加入a g的铜粉,搅拌使之全部溶解,溶液中一定有的阳离子是______,可能有的阳离子是。发生反应的离子方程式为;
(2)再向上述溶液中加入 b g铁粉,充分反应后过滤得滤渣c g,可能发生反应的离子方程式为。若已知 a>c,则 c克滤渣是_________。