(15分)目前,“低碳经济”备受关注,CO2的产生及有效开发利用成为科学家研究的重要课题。
(1)向浓CaCl2溶液中通入NH3和CO2,可以制得纳米级碳酸钙(粒子直径在1〜10nm之间)。
①向浓CaCl2溶液中通入NH3和CO2气体制纳米级碳酸钙时,应先通入NH3,后通 入CO2。制备纳米级碳酸钙的离子方程式为______________
②判断产品中是否含有纳米级碳酸钙的实验方法为_____________。
(2)—定条件下,C(s)和H2O(g)反应,能生成CO2(g)和H2(g)。将C(s)和H2O(g)分别加入甲、乙两个密闭容器中,发生反应:C(s)+2H2O(g) CO2(g)+2H2(g),其相关数据如下表所示:
CO2(g)+2H2(g),其相关数据如下表所示: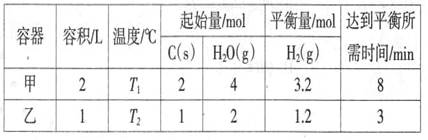
①T10C时,该反应的平衡常数K=_______
②乙容器中,当反应进行到1.5min时,H20(g)的物质的量浓度_______ (填选项字母)。
A.=0.8 mol/L B.-1.4 mol/L
C.<1.4 mol/L D.>1.4 mol/L
③丙容器的容积为1L,t20C时,起始充入a mol C02和bmol H2(g),反应达到平衡时,测得CO2的转化率大于H2的转化率,则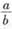 的值需满足的条件为______________;
的值需满足的条件为______________;
④丁容器的容积为1L,T10C时,按下列配比充入C(s)、H2O(g)、CO2(g)和H2(g),达到平衡时各气体的体积分数与甲容器完全相同的是_______(填选项字母)。
A.0.6 mol、1.0 mol、0.5 mol、1.0 mol
B.0.6 mol、2.0 mol、O mol、O mol
C.1.0 mol、2.0 mol、1.0 mol、2.0 mol
D.0.25 mol、0.5 mol、0.75 mol、1.5 mol
(3)CO2在一定条件下可转化为甲醚(CH3OCH3)。用甲醚燃料电池做电源,用惰性电极电解饱和K2SO4溶液可制取H2SO4和KOH,实验装置如下图所示:
①甲醚燃料电池的负极反应式为________
②A口导出的物质为_____________________(填化学式)。
③若燃料电池通入CH3OCH3(g)的速率为0.1mol/min-1 ,2 min时,理论上C口收集到标准状况下气体的体积为______________
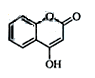 是一种医药中间体,常用来制备抗凝血药,可通过下列路线合成:
是一种医药中间体,常用来制备抗凝血药,可通过下列路线合成: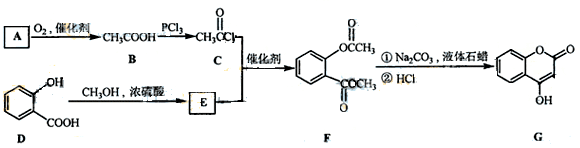 (1)A与银氨溶液反应有银镜生成,则A的结构简式是。
(1)A与银氨溶液反应有银镜生成,则A的结构简式是。
(2)B→C的反应类型是。
(3)E的结构简式是。
(4)写出F和过量NaOH溶液共热时反应的化学方程式:
。
(5)下列关于G的说法正确的是
a.能与溴单质反应 b. 能与金属钠反应
c. 1molG最多能和3mol氢气反应 d. 分子式是C9H6O3
某中性有机物A的化学式为C6H12O2,可发生如图所示变化:
(1)若C、E均能发生银镜反应,则A的结构简式可能有:
、 、
、
、。
(2)若C、E均不能发生银镜反应,则A的结构简式可能有:
_____________________________、。
今有化合物甲:
(1)请写出丙中含氧官能团的名称:_____________________。
(2)请判别上述哪些化合物互为同分异构体:_______________。
(3)请分别写出鉴别甲、乙、丙化合物的方法(指明所选试剂及主要现象即可)。
鉴别甲的方法:____________________________________。
鉴 别乙的方法:____________________________________。
别乙的方法:____________________________________。
鉴别丙的方法:____________________________________。
(4)请按酸性由强至弱排列甲、乙、丙的顺序:_______________________。
I.在实验室利用下列装置,可制备某些气体并验证其化学性质。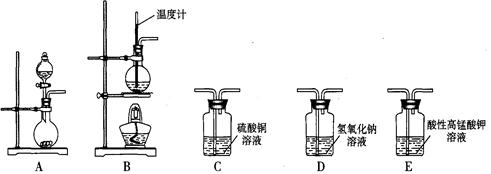
完成下列表格:
| 序号 |
气体 |
装置连接顺序(填字母) |
制备反应的化学方程式 |
| (1) |
乙烯 |
__________________ |
_________________________ |
| (2) |
乙炔 |
A→C→E |
_________________________ |
II. (1)工业上用乙烯和氯气为原料,经下列各步合成聚氯乙烯(PVC):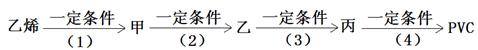
反应(2)的化学方程式是__________________________________________;
PVC的结构简式是_________________________________________________。
(2)石油被称为“工业血液”。A是从石油中得到的链状烃,相对分子质量为42。以A为原料,利用下述反应合成甘油,在方框内填上中间体的结构简式。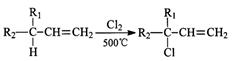
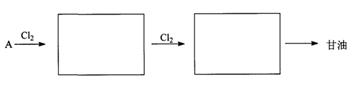
将4 g NaOH溶于_________g 水中,可使溶液中H2O与Na+的物质的量之比为20:1,此溶液中溶质的质量分数为;若测得该溶液的密度为1.1 g·cm-3,则该溶液体积为(精确到小数点后1位),溶液中c(Na+)为_________(精确到小数点后2位)。