下列叙述中,不能用平衡移动原理解释的是 ( )
| A.红棕色的NO2,加压后颜色先变深后变浅 |
| B.由H2、I2(g)、HI(g)气体组成的平衡体系加压后颜色变深 |
| C.高压比常压有利于合成SO3的反应 |
| D.黄绿色的氯水光照后颜色变浅 |
纯铁的熔点为1535 ℃,而在高炉中炼铁时生铁(含碳量较高的铁的合金)在1200 ℃左右就熔化了,这是因为
| A.铁的纯度高,所以熔点变低 | B.形成了铁碳合金,所以熔点变低 |
| C.合金的熔点高于它的成分金属 | D.生铁在高炉内熔化的过程中发生了化学变化 |
用坩埚钳夹住一小块刚用酸处理过的铝箔,在酒精灯上加热至熔化,发现熔化的铝并不滴落。下列关于上述实验现象的解释不正确的是
| A.铝在空气中能很快形成氧化膜 |
| B.金属铝活动性较弱,不能在空气中燃烧 |
| C.氧化铝的熔点比铝高 |
| D.氧化铝薄膜包住了熔化的铝 |
化合物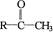 与NaOH溶液、碘水三者混和后可发生如下反应:
与NaOH溶液、碘水三者混和后可发生如下反应:
①I2 + 2NaOH ="=" NaI + NaIO + H2O
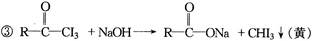
此反应称为碘仿反应,根据上述反应方程式,推断下列物质中能发生碘仿反应的有
| A.CH3CH2COCH2CH3 | B.CH3COCH2CH3 |
| C.CH3CH2COOCH3 | D.CH3OOCH |
某同学按右图所示的装置进行实验。 A、B为两种常见金属,它们的硫酸盐可溶于水。当 K 闭合时,在交换膜处 SO42一从右向左移动。下列分析正确的是
A.溶液中A2+浓度减小
B.B 的电极反应: B-2eˉ==B2+
C.y 电极上有 H2产生,发生还原反应
D.反应初期, x电极周围出现白色胶状沉淀,不久沉淀溶解
如右图所示,A池用石墨电极电解氢氧化钠溶液,B池精炼粗铜,一段时间后停止通电,A池D极产生的气体在标准状况下为2.24 L。下列说法正确的是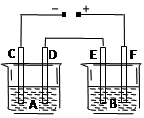
| A.A池为电解池,B池为原电池 |
| B.D电极与E电极都发生氧化反应 |
| C.F极是以粗铜板为材料作阳极 |
| D.B池中E极质量增加12.8 g |