S(单斜)和S(正交)是硫的两种同素异形体。
已知:① S(单斜,s)+O2(g) === SO2(g) △H1=-297.16 kJ·mol-1
② S(正交,s)+O2(g) === SO2(g) △H2=-296.83 kJ·mol-1
③ S(单斜,s) === S(正交,s) △H3
下列说法正确的是( )
| A.△H3=+0.33 kJ·mol-1 |
| B.单斜硫转化为正交硫的反应是吸热反应 |
| C.S(单斜,s)===S(正交,s) △H3<0,正交硫比单斜硫稳定 |
| D.S(单斜,s)===S(正交,s) △H3<0,单斜硫比正交硫稳定 |
某澄清透明溶液中可能含有①Al3+;②Mg2+;③Fe3+;④Fe2+;⑤H+;⑥C032-⑦NO3-中的几种,向该溶液中逐滴加入NaOH溶液至过量,生成沉淀的质量与NaOH的物质的量的关系如图所示。则该溶液中一定含有的离子是: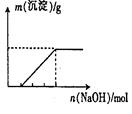
| A.②⑤⑥⑦ | B.②③⑤⑦ |
| C.①②③⑥⑦ | D.①②③④⑤⑦ |
下列表示对应化学反应的离子方程式正确的是:
| A.将过量SO2气体通入氨水中:SO2+2 NH3·H2O ="2" NH4+ + SO32-+H2O |
| B.向FeI2溶液中通入足量的氯气:2Fe2++2I-+2Cl2===2Fe3++I2+4Cl- |
| C.向氢氧化钡溶液中逐滴加入少量碳酸氢钠溶液:Ba2++2OH-+2HCO3- = BaCO3↓+2H2O+ CO32- |
| D.硝酸铁溶液中滴加足量HI溶液:Fe3+ + 3NO3-+12H+ +10I- = Fe2+ + 5I2 + 3NO↑ + 6H2O |
有一反应:2A+B 2C,其中A、B、C均为气体,右图中的曲线是该反应在不同温度下的平衡曲线,x轴表示温度,y轴表示B的转化率,图中有a、b、c三点,如图所示,则下列描述正确的是:
2C,其中A、B、C均为气体,右图中的曲线是该反应在不同温度下的平衡曲线,x轴表示温度,y轴表示B的转化率,图中有a、b、c三点,如图所示,则下列描述正确的是: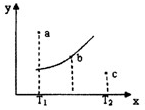
A.该反应是放热反应
B.b点时混合气体的平均摩尔质量不再变化
C.T1温度下a点表示若想达到平衡,可以采取增大压强的方法
D.c点可表示v(正)<v(逆)
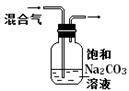
下列图中的实验方案,能达到实验目的的是:
| A |
B |
C |
D |
|
| 实验 方案 |
 |
 |
 |
 |
| 实验 目的 |
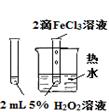
验证FeCl3对H2O2分解反应有催化作用 |
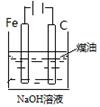
制备Fe(OH)2并能较长时间观察其颜色 |
除去CO2气体中混有的SO2 |
比较HCl、H2CO3和H2SiO3的酸性强弱 |
用惰性电极电解 M(NO3)x的水溶液, 当阴极上增重a g时, 在阳极上同时产生b L氧气( 标准状况),从而可知 M 的原子量为:
A.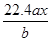 |
B. |
C.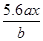 |
D. |