下列有关铝化合物说法正确的是( )
| A.氧化铝的熔点很高,所以不可以用来冶炼铝 |
| B.氢氧化铝是一种胶状沉淀,有较大表面积,有吸附性,可用作净水剂 |
| C.实验室可以用氢氧化钠与氯化铝来制备氢氧化铝 |
| D.氢氧化铝既可与强酸反应又可与强碱反应,是两性氢氧化物 |
A、B、C三种短周期元素在元素周期表中的相对位置如图所示,已知A、C可分别与B形成化合物X和Y,A与B的质子数之和为C的质子数,现有以下说法,其中判断正确的组合是()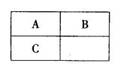
①B与C均存在同素异形体
②X的种类比Y的多
③沸点:A的氢化物小于C的氢化物
④C的最高价氧化物对应水化物能与A的氢化物形成三种盐
A.①②③④ B.②③ C.①②④ D.①④
下列实验装置设计正确,且能达到目的的是()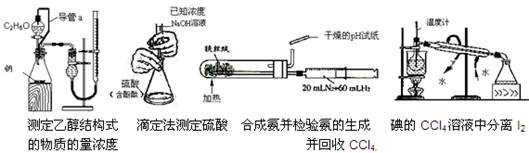
A B C D
对下列事实的解释错误的是()
| A.用75%的乙醇溶液进行消毒,是由于乙醇能使蛋白质变性 |
| B.医疗上用硫酸钡作“钡餐”,是由于硫酸钡难溶于水 |
| C.用氢氟酸雕刻玻璃,是由于氢氟酸能与二氧化硅反应 |
| D.向Na2O2与水完全反应后的溶液中加MnO2,产生O2,是由于该溶液中含H2O2 |
下列离子方程式中,正确的是()
| A.向次氯酸钙溶液中通入少量二氧化硫: Ca2++2ClO-+SO2+H2O==CaSO3↓+2HClO |
| B.用Na2CO3溶液作洗涤剂:CO32- + 2H2O H2CO3 + 2OH- |
| C.用碳酸钠溶液吸收少量二氧化硫: 2CO32-+SO2+H2O ==2HCO3-+SO32- |
| D.酸性条件下KIO3溶液与KI溶液发生反应生成I2: IO3-+5I-+3H2O=3I2+6OH- |
用NA表示阿伏加德罗常数的值。下列叙述正确的是()
| A.1molFeCl3和沸水完全反应转化为氢氧化铁胶体后,其中胶体粒子数目为NA |
| B.标准状况下,1L液态水中含有的H+ 数目10-7NA |
| C.CO和N2为等电子体,22.4L的CO气体与lmol N2所含的电子数相等 |
| D.13.0 g锌与一定量浓硫酸恰好完全反应,生成气体分子数为0.2NA |