下列各组物质中分子数一定相同的是
| A.2 g O3和2g O2 |
| B.9g H2O和0.5NA个CO2 |
| C.标准状况下1 mol O2和22.4 L H2O |
| D.0.2 mol H2和4.48 L HCl |
Murad等三位教授最早提出了NO分子在人体内有独特功能,近年来此领域研究有很大进展,因此这三位教授荣获了1998年诺贝尔医学及生理学奖,关于NO的下叙述不正确的
| A.NO可以是某些低价N物质被氧化产物 |
| B.NO能导致臭氧层空洞 |
| C.NO可以是某些高价N物质被还原产物 |
| D.NO是红棕色气体 |
飘尘是物质燃烧时产生的粒状漂浮物,颗粒很小,不易沉降。它与空气中的SO2和O2接触时,SO2会部分转化为SO3,使空气的酸度增加,环境污染更为严重。其中飘尘所起的作用可能是:
| A.氧化剂 | B.还原剂 | C.催化剂 | D.载体 |
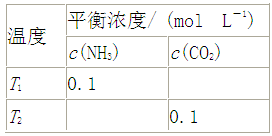
将一定量的氨基甲酸铵固体置于某容积恒定的真空容器中,发生反应: H2NCOONH4(s) 2NH3(g)+CO2(g)。在不同温度下,该反应平衡状态部分数据下表。下列说法正确的是()
2NH3(g)+CO2(g)。在不同温度下,该反应平衡状态部分数据下表。下列说法正确的是()
| A.若T2>T1,则该反应的ΔH<0 |
| B.向容器中充入N2,H2NCOONH4质量增加 |
| C.NH3体积分数不变时,说明该反应达到平衡 |
| D.T1、T2时,H2NCOONH4转化的物质的量:Δn(T2)=2Δn(T1) |
将pH=1的盐酸平均分成两份,一份加适量水,另一份加入与该盐酸物质的量浓度相同的适量NaOH溶液后(设混合后溶液体积的微小变化忽略不计),pH都升高了1,则加入的水与NaOH溶液的体积比为()
| A.9:1 | B.10:1 | C.11:1 | D.12:1 |
化合物HIn在水溶液中因存在以下电离平衡,故可用作酸碱指示剂
HIn(溶液)  H+(溶液)+In-(溶液)
H+(溶液)+In-(溶液)
红色黄色
浓度为0.02 mol·L-1的下列各溶液 ①盐酸 ②石灰水 ③NaCl溶液 ④NaHSO4溶液 ⑤NaHCO3溶液 ⑥氨水,其中能使指示剂显红色的是()
| A.②⑤⑥ | B.①④ | C.①④⑤ | D.②③⑥ |