下列物质都是常见的食品添加剂,可用作防腐剂但必须严格控制用量的是
| A.食盐 | B.亚硝酸钠 | C.蔗糖 | D.味精(谷氨酸钠) |
下列叙述中,正确的是
| A.用丁达尔现象实验可以区分食盐水和淀粉溶液 |
| B.氨气的水溶液能导电,所以氨气是电解质 |
| C.NO2、SO2溶于水都发生氧化还原反应 |
| D.Fe分别与氯气和稀盐酸反应可得到同一种氯化物 |
N、O、Si、S是重要的非金属元素,下列说法正确的是
| A.N、O、S、Si的原子半径逐渐增大,非金属性逐渐减弱 |
| B.氮的氧化物和硫的氧化物既是形成光化学烟雾,又是形成酸雨的主要物质 |
| C.S、SO2和Si、SiO2四种物质均能与NaOH溶液反应,各自又能与某些酸反应 |
| D.N、Si、S的单质均能和氧气反应,生成的产物分别是NO2、SiO2和SO2 |
下列有关化学实验叙述正确的是
| A.容量瓶、滴定管、分液漏斗使用前都必须检查是否漏水 |
| B.用98%的浓硫酸配制100g10%的稀硫酸时,除使用量筒外还需用到容量瓶 |
| C.在钠跟水反应的实验中,切下绿豆粒大小的钠投入水中进行实验,剩余的钠块丢弃到废料桶中 |
| D.若FeCl2溶液中含有I-杂质,可用过量Cl2氧化后进行萃取分液 |
下列离子方程式正确的是
A.钠与水反应: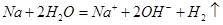 |
B.硅酸钠溶液与醋酸溶液混合: + +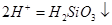 |
C.0.01mol/LNH4Al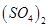 溶液与0.02mol/LBa(OH)2溶液等体积混合: 溶液与0.02mol/LBa(OH)2溶液等体积混合: 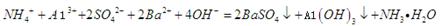 |
D.向次氯酸钙溶液通入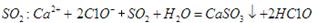 |
下列有关溶液组成的描述合理的是
A.无色透明的溶液中: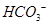 、K+、Na+、MnO4- 、K+、Na+、MnO4- |
B.酸性溶液中可能大量存在Na+、ClO 、SO42-、I 、SO42-、I |
C.含有0.1 mol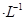 Fe3+ 的溶液中可以大量存在:K+、Mg2+、I-、NO3- Fe3+ 的溶液中可以大量存在:K+、Mg2+、I-、NO3- |
| D.室温下,PH=l的溶液中一定可以存在:Na+、Fe3+、NO3-、SO42- |