(5分)元素周期表是学习化学的重要工具。下面是元素周期表中1~18号元素原子核外电子排布,我们对它进行研究:
⑴第16号元素属于_______元素(填“金属”或“非金属”),它在化学反应中容易________(填“得”或“失”)电子;
⑵ 元素的化学性质与原子结构中的______________数关系密切;
⑶在同一族中,各元素的原子结构呈现的规律有________________ (任写一点);
⑷研究表明:第二周期从3~9号元素的原子电子层数相同,核电荷数逐渐增大,核对核外电子的引力逐渐增大,故原子半径逐渐减小。我分析第三周期从11~17号元素原子半径变化规律是 _________________________________。
化学与健康息息相关。
(1)“合理膳食,均衡营养”会让我们更健康。
①下列食品中富含糖类的是______(填序号,下同)。
A.鸡蛋 B.馒头 C.蔬菜
②为了预防佝偻病和发育不良,幼儿及青少年可以补充一些含______元素的食品。
(2)生活中的下列做法,不利于人体健康的是______。
A.食用霉变的花生
B.倡导大家不吸烟
C.食用甲醛溶液浸泡的海产品
兴趣小组根据老师提供的实验装置进行如下实验,U型管左侧管内固定一小试管,右侧管内挂的是紫色石蕊试液浸泡过的滤纸条,其中一条是湿润的,一条是干燥的。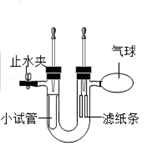
(1)将左侧胶头滴管中的稀硫酸注入装有碳酸钠粉末的小试管中,写出小试管中发生反应的化学方程式__________。证明二氧化碳可与水反应的现象是__________,发生反应的化学方程式为__________。
(2)将右侧胶头滴管内的药品注入U形管内,观察到气球明显变瘪,则右侧胶头滴管中的药品为__________,发生反应的化学方程式为__________。
下图所示装置均可用于测定空气中氧气的含量。
(1)图甲实验中,红磷燃烧的化学方程式为_________________。
(2)某化学小组对该实验进行改进(装置如图乙所示),用暖宝宝发热剂代替红磷,发热剂是铁粉、水和食盐等。下列说法中,错误的是________。
| A.此实验的原理是利用铁生锈消耗氧气 |
| B.实验前一定要检查装置的气密性 |
| C.此实验中发热剂的多少不影响测量结果 |
| D.此实验测出氧气的体积分数约是18.3% |
水在实验室中有不同用途。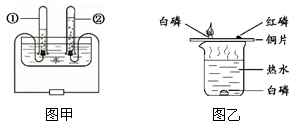
(1)图甲为电解水的装置图,其反应方程式是__________;试管①中收集的气体是__________。
(2)图乙为探究燃烧条件实验,其中热水作用__________。
根据下图回答问题。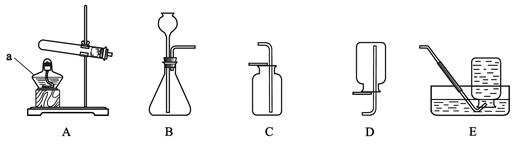
(1)仪器a的名称是______。
(2)实验室用高锰酸钾制取氧气的化学方程式是______,选用的收集装置是______。
(3)实验室用大理石和稀盐酸制取二氧化碳的化学反应方程式为_______________,选用的发生装置是_____。