用过量的H2SO4、NaOH、NH3·H2O、NaCl等溶液,按右图所示步骤分开五种离子。则溶液①、②、③、④是( )
| A.①NaCl ②NaOH ③NH3·H2O ④H2SO4 |
| B.①NaCl ②NH3·H2O ③NaOH ④H2SO4 |
| C.①H2SO4②NaOH ③NH3·H2O ④NaCl |
| D.①H2SO4 ②NH3·H2O ③NaOH ④NaCl |
乙基香草醛是食品添加剂的增香原料,其结构简式如右图所示,下列对该物质叙述正确的是()
| A.该物质可以进行消去反应 |
| B.该物质可以进行水解反应 |
| C.1mol该物质最多可与3 mol H2反应 |
| D.该物质可以和溴水发生取代反应 |
简单原子的原子结构可用下图所示方法形象地表示: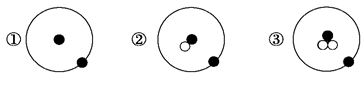
其中●表示质子或电子,○表示中子,则下列有关①②③的叙述正确的是 ( )
| A.①②③互为同位素 | B.①②③互为同素异形体 |
| C.①②③是三种化学性质不同的粒子 | D.①②③具有相同的质量数 |
具有相同电子层结构的三种微粒An+、Bn-和C,下列分析正确的是( )
A.原子序数关系:C>B>A
B.微粒半径关系:r(Bn-)<r(An+)
C.微粒C是稀有气体元素的原子
D.原子半径关系是:r(A)<r(B)<r(C)
下列叙述中,正确的是 ( )
| A.在一个基态多电子的原子中,可以有两个运动状态完全相同的电子 |
| B.在一个基态多电子的原子中,不可能有两个能量完全相同的电子 |
| C.在一个基态多电子的原子中,M层上的电子能量肯定比L层上的电子能量高 |
| D.如果某一基态3p能级上仅有2个电子,它们自旋方向必然相反 |
桶烯(Barrelene)结构简式如图所示,则下列有关说法不正确的是()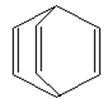
| A.桶烯分子中所有原子在同一平面内 |
| B.桶烯在一定条件下能发生加成反应和加聚反应 |
| C.桶烯与苯乙烯(C6H5CH=CH2)互为同分异构体 |
| D.桶烯中的一个氢原子被氯原子取代,所得产物只有两种 |