比较和归纳是学习化学的常用方法。某学习小组的同学在下图所列出的实验装置的基础上,对二氧化碳的制取进行研究。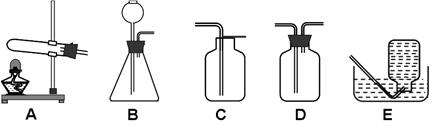
(1)确定气体发生装置应考虑的因素是 和 。
(2)甲同学用大理石与稀盐酸反应制取二氧化碳气体,化学方程式是:
,要得到一瓶干燥的二氧化碳气体,所选装置的连接顺序是 (填字母),可选用 作干燥剂。
(3)加热固体碳酸氢钠或固体碳酸氢铵都能产生二氧化碳气体,化学反应方程式分别是:2NaHCO3  Na2CO3+ H2O+ CO2↑; NH4HCO3
Na2CO3+ H2O+ CO2↑; NH4HCO3  NH3↑+ H2O+ CO2↑ 乙同学选择加热碳酸氢钠的反应制取二氧化碳,则发生装置应选用 (填字母)。他不选择加热碳酸氢铵制取二氧化碳的理由是
NH3↑+ H2O+ CO2↑ 乙同学选择加热碳酸氢钠的反应制取二氧化碳,则发生装置应选用 (填字母)。他不选择加热碳酸氢铵制取二氧化碳的理由是
化学是一门以实验为基础的自然科学,下图所示实验是我们所熟悉的。
甲乙丙
(1)图甲所示实验用于测定空气中氧气的体积分数。红磷在空气中燃烧的化学方程式是。关于该实验的下列说法中,正确的是(填字母序号)。
| A.实验时红磷一定要足量 |
| B.点燃红磷前先用弹簧夹夹紧乳胶管 |
| C.红磷熄灭后立刻打开弹簧夹 |
| D.最终进入瓶中水的体积约为氧气的体积 |
E.该实验必须检查装置的气密性
(2) 同学们用乙所示实验探究化学反应前后物质的质量关系。如果a、b分别是铁钉和硫酸铜溶液,与分别是锌和稀盐酸(已知:Fe+CuSO4  FeSO4+Cu Zn+2HCl
FeSO4+Cu Zn+2HCl ZnCl2+H2↑),测定结果不同的原因是。
ZnCl2+H2↑),测定结果不同的原因是。
(3)如图丙所示,某化学课外小组将紫色石蕊试液浸泡并晾干的紫色纸人,进行以下实验:
①左右两袖分别用毛笔涂上稀醋酸和稀盐酸,可观察到两袖均变红色;
②将“c”裤腿涂上蒸馏水;
③将纸人放入盛有干燥二氧化碳气体的集气瓶中;
④将纸人取出用热宝加热。
回答下列问题:
Ⅰ. 解释步骤③中“c”裤腿呈红色的原因(用化学方程式表示)。
Ⅱ. 步骤④中未看到两袖有明显变化,你认为其他部位可能观察到的现象及原因是。
为制取并收集一瓶干燥的CO2气体,某课外研究小组向实验教师领取了下列仪器和药品:
(1)写出编号仪器的名称①_____________;⑥_______________。要完成该实验,他们还必须向实验老师领取的仪器有镊子和___________。
(2)实验室制取时CO2发生反应的化学方程式为_________________________________。
(3)收集CO2时,他们如何检验已CO2收集满?_________________________________;
(4)实验室制取气体要选择适当反应物。我们知道实验室制取大量CO2气体不能用浓盐酸,因为_______________________;也不能用稀硫酸,因为______________________。
(5)他们对实验室制取CO2的实验条件展开了进一步的探究,做了如下四个对比实验:
①取m g块状大理石与足量的溶质质量分数为5%的盐酸反应;
②取m g块状大理石与足量的溶质质量分数为10%的盐酸反应。
实验现象:产生气泡的快慢顺序为②>①
实验结论:影响大理石和盐酸反应快慢的因素有_______________________________。
用木炭还原氧化铜的实验如图所示。
(1)酒精灯加网罩的目的是;
(2)刚开始预热,试管②中立即产生气泡,但石灰水
不变浑浊,原因是;
(3)继续加热,观察到试管①中的现是;
(4)请写出试管①中发生反应的化学方程式是:。
氢氧化钠、氢氧化钙都是实验室常用的碱。
(1)要鉴别氢氧化钠稀溶液和饱和氢氧化钙溶液,下列方法不能够达到目的的是______(填序号)。
| A.分别滴加碳酸钠溶液 |
| B.分别通入二氧化碳 |
| C.分别滴加稀盐酸 |
| D.分别加热原溶液至80℃ |
(2)同学们将饱和氢氧化钙溶液与碳酸钠溶液混合,过滤得到滤渣和滤液。同时对滤液中溶质的成分进行了进一步探究:
【猜想与假设】甲同学认为:可能是NaOH、Na2CO3、Ca(OH)2;
乙同学认为:可能是NaOH、Na2CO3;
丙同学认为:可能是NaOH、Ca(OH)2;
丁同学认为:可能是______________(填化学式)。
【交流与评价】经过讨论,大家一致认为_______同学的猜想不合理。理由是_____________。
【实验与探究】(1)乙同学取原滤液,向其中倾倒足量的稀盐酸,观察到有大量气泡产生,于是得出该滤液中溶质是NaOH、Na2CO3的结论,证实了自己的猜想。
(2)丙同学取原滤液向其中通入足量的CO2,溶液____________现象(填“有”或“没有”),据此否定了自己的猜想。
(3)丁同学为了验证乙同学结论也取原滤液向其中滴加了少量稀盐酸,却发现无气泡产生。
【解释与结论】大家经过分析找出了丁同学所用试剂与乙同学相同,却没有看到气泡的原因。你认为可能的原因是__________________。
为了对浓硫酸腐蚀性有个深刻的认识,化学活动小组进行了下列实验探究。请你也将活动记录补充完整。
实验题目:浓硫酸的腐蚀性实验探究
【实验用品】浓硫酸、小木条、玻璃片
| 实验步骤 |
实验现象 |
结论 |
| (1) |
(2) |
浓硫酸有强烈的腐蚀性,使用时应十分小心。 |
【反思与交流】化工厂生产的硫酸是浓硫酸,实际应用需要各种浓度的稀硫酸,稀释时应正确操作。如在实验室稀释浓硫酸时,应先向烧杯中加入适量的______________,再沿烧杯内壁缓缓加入______________________,并用玻璃棒不断搅拌,使产生的热量迅速扩散。如果不慎将浓硫酸沾在皮肤上,应____________________。