X、Y、Z是ⅠAⅦA族的三种非金属元素,它们在周期表中的位置如右图所示。试完成下列问题: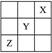
(1)X元素单质的化学式是__________。
(2)Y元素的原子结构示意图是__________,Y与Na所形成化合物的电子式为__________。
(3)Z元素的名称是__________,从元素原子得失电子的角度看,Z元素具有__________性;若从Z元素在周期表中所处位置看,它具有这种性质的原因是____________________,其价电子排布式为__________。
常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
| 实验编号 |
HA物质的量浓度(mol·L-1) |
NaOH物质的量浓度(mol·L-1) |
混合溶液的pH |
| 甲 |
0.2 |
0.2 |
pH=a |
| 乙 |
C |
0.2 |
pH=7 |
| 丙 |
0.2 |
0.1 |
pH>7 |
| 丁 |
0.1 |
0.1 |
pH=9 |
请回答:(1)不考虑其它组的实验结果,单从甲组情况分析,如何用a (混合溶液的pH)来说明HA是强酸还是弱酸。
(2)不考虑其它组的实验结果,单从乙组情况分析,C是否一定等于0.2(选填“是”或“否”)。混合液中离子浓度c(A-)与 c(Na+)的大小关系是。
A.前者大 B.后者大 C.二者相等 D.无法判断
(3)从丙组实验结果分析,HA是酸(选填“强”或“弱”)。该混合溶液中离子浓度由大到小的顺序是。(4)丁组实验所得混合溶液中由水电离出的c(OH-)=mol·L-1。写出该混合溶液中下列算式的精确结果(不能做近似计算): c(Na+)-c(A-)=mol·L-1, c(OH-)-c(HA)=mol·L-1。
在75℃左右,用HgSO4作催化剂,乙炔可水化为乙醛.但HgSO4遇到某些特定物质常会发生催化剂中毒而失去催化作用,H2S就是其中一种.现用乙炔水化法,只用块状电石、浓硫酸、水、NaOH溶液、HgO粉末五种物质制乙醛,装置如图: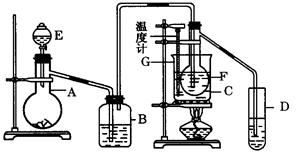
请回答以下问题:
(1) 实验开始时,仪器A中盛放电石,B中应装入,其作用是.
(2) 仪器D中盛放水,其作用是.
(3) 蒸馏烧瓶F中应加入HgO和另外两种试剂,若将三者分别直接加入,请按加入的先
后顺序写出包括HgO在内的各试剂名称,将HgO加入F中的操作方法是.
(4) 装置图中,加热F的方式叫,所选用温度计G的量程表示正确的是__________(填代号).
| A.0℃~50℃ | B.0℃~100℃ | C.0℃~200℃ | D.0℃~360℃ |
(5) 检验乙醛已制出的操作、现象是.
已知有机分子中烯键可以在一定的条件下发生臭氧分解反应,例如: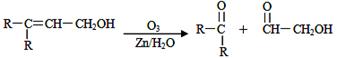 ,某有机物A的化学式是
,某有机物A的化学式是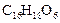 ,它可以在一定条件下合成一种感光性高分子材料,该材料在微电子工业上具有重要用途.
,它可以在一定条件下合成一种感光性高分子材料,该材料在微电子工业上具有重要用途.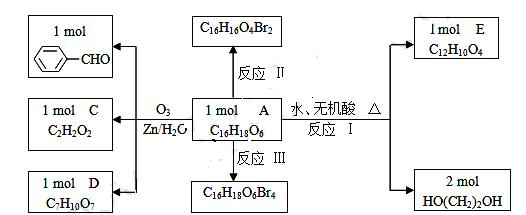
请回答:
(1) 指出下列反应的反应类型.反应II_____________;反应III_____________.
(2) 根据上述信息判断A中含有的官能团(或名称)______________________________.
(3) 写出下列物质的结构简式:C;D______________.
(4) 写出反应III的化学反应方程式(必须用结构简式表示):
____________________________________________________________________________
已知A为固态物质,实验室利用A与水反应制备气态物质B;F遇到FeCl3溶液显紫色;I 属于二元醇.各物质间的转化关系如下图所示:
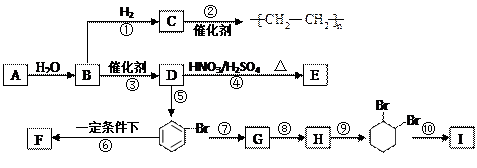 |
(1)请写出A的电子式____________________;反应⑤中加入的试剂是 .
写出结构简式: E ; F ;G ;H .
(2)以上各步反应中属于加成反应的有: ;属于取代反应的有: ;属于消去反应的有: ;属于聚合反应的有: 。(用序号填空)
(3)写出下列化学反应方程式
反应②________________________________________________________
反应④_______________________________________________________
反应⑧_______________________________________________________
反应⑩________________________________________________________
(4)写出1mol 物质I与足量的醋酸在浓硫酸加热条件下充分反应生成二元酯的方程式:
_________________________________________________________
写出F与Na2CO3溶液反应的离子方程式:
____________________________________________________________________________
(5)已知物质B在一定条件下可以转变成甲醛,请写出甲醛与银氨溶液反应的离子方程式:
__________________________________________________________
现有A、B、C、D、E五种烃.已知
① 1 mol五种烃分别完全燃烧,都生成134.4 L CO2(标准状况);且烃C完全燃烧时,生成的水的物质的量比CO2多;
② A和D都能使溴水褪色,其中1 mol D可以和1 mol H2反应生成1 mol A;1 mol A又可继续和1 mol H2 反应又生成1 mol C;
③ C不与溴水或酸性KMnO4溶液反应;
④ A存在多种同分异构体,其中C只能由一种A与氢气反应而得;
⑤ B在铁屑存在下可以跟液溴反应,但不与溴水或酸性高锰酸钾溶液反应;
⑥ B能和氢气充分反应生成E;
请回答下列问题:
(1)写出所属烃的类别:A___________,B___________,C___________.
(2)烃C的一卤代产物有种同分异构体.
(3)用“系统命名法”对D命名:.
(4)以上几种物质能作为溴水中溴的萃取剂的有:(用“A、B、C……”作答).
(5)写出符合题设条件的A与HCl在催化剂作用下的加成反应方程式:_________________.