(1)中学教材上所示的NaCl晶体结构,它向三维空间延伸,得到完美晶体。NiO(氧化镍)晶体的结构与NaCl相同,Ni2+与最邻近O2-的核间距离为a×10-8cm,计算NiO晶体的密度(已知NiO的摩尔质量为74.7 g·mol-1)。
(2)天然的和绝大部分人工制备的晶体都存在各种缺陷,例如在某种NiO晶体中就存在如图所示的缺陷:一个Ni2+空缺,另有两个Ni2+被两个Ni3+所取代。其结果晶体仍呈电中性,但化合物中Ni和O的比值却发生了变化。其氧化镍样品组成为Ni0.97O,试计算该晶体中Ni2+与Ni3+的离子数之比。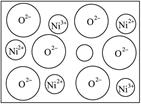
将某种碳酸钠晶体(Na2CO3 · nH2O)和碳酸氢钠的混合物11.24 g,加热到质量不再减少,剩余残渣8.48 g 。加热时产生的气体依次通过浓H2SO4和NaOH溶液后,NaOH溶液增重1.32 g(假设气体全部被吸收)。试计算:
(1)混合物中NaHCO3的质量分数为% 。
(2)混合物中碳酸钠晶体与碳酸氢钠的物质的量之比为。(写出计算过程)
将标准状况下44.8 L NH3与足量的盐酸充分反应。试计算:
(1)生成NH4Cl的物质的量为多少?
(2)生成NH4Cl的质量为多少?
把0.6 mol X气体和0.6 mol Y气体混合于2 L密闭容器中,它们发生如下反应:
2X(g)+Y(g) = nZ(g)+2W(g) 。2 min 末已生成0.2 mol W ,若以Z的浓度变化表示的反应速率为0.1 mol·L-1·min-1,计算:
(1)化学反应方程式中n的值是多少?
(2)2 min末时Y的浓度?
在一体积固定的密封容器中加入反应物A、B,发生如下反应:A+2B=3C。反应经2min后,A的浓度从开始的1.0mol/L降到0.8mol/L。已知反应开始时B的浓度是1.2mol·L-1,求:(1)2min末B、C的浓度?
(2)以单位时间内A的浓度的减小来表示2min内该反应的平均速率?
将5.13g Ba(OH)2粉末加入100 ml硫酸和盐酸的混合液中,充分反应至沉淀不再生成时,过滤得干燥沉淀5.825g。取滤液20ml跟足量铁粉反应,生成22.4ml(标准状况下)气体。求:
⑴滤液的pH
⑵原混合液中c(Clˉ)、c(SO42ˉ)。