某兴趣小组话动中,同学们按图1装置对“可燃物燃烧的条件”进行探究。探究过程中,大家对磷燃烧生成的大量白烟是否危害人体健康提出疑问。
【查阅资料】白磷的着火点是40℃,红磷的着火点是240℃,……燃烧产物五氧化二磷是白色固体,会刺激人体呼吸道,并能与空气中的水蒸气反应,生成有毒的偏磷酸(HPO3)。
【交流与讨论】白烟对人体健康有害,该实验装置必须改进。
【改进与实验】同学们按改进后的图2装置进行实验。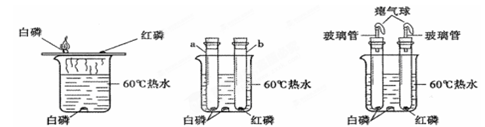
图1 图2 图3
请你帮助他们将下表补充完整。
| 实验现象 |
对实验现象的解释 |
| (1)a试管中白磷燃烧,热水中白磷没有燃烧 |
(1)热水中白磷没有燃烧的原因是热水中的白磷没有与氧气(或空气)接触。 |
| (2)b试管中红磷没有燃烧 |
(2)b试管中红磷没有燃烧的原因是 。 |
【反思与评价】
(1)根据上述实验得出,可燃物燃烧的条件是 。
(2)同学按图2完成实验后,经反思总结实验过程,又改进设计了图3实验,其中图3实验中气球的作用是 (填字母)。
A.收集生成的气体
B.防止有害物质污染空气
C.调节试管内的气体压强,避免橡皮塞因试管内气体热膨胀而松动
【拓展与迁移】实验小结时,小朱同学说:“待a试管冷却后,如果将试管口朝下垂直伸入水面下(室温),并取下橡皮塞,将看到液体进入试管。”这一说法得到大家的一致认同。你认为如果不考虑橡皮塞占试管的容积,实验所用白磷足量,装置气密性良好,且进入a试管内液体的体积约占试管容积的1∕5,这一现象还可以得出的结论是 。
铝制品在日常生活中应用广泛,但铝制品却不宜长时间盛放腌制食品。资料显示:"铝制品表面虽然有一层致密的氧化膜保护……氯化钠也会破坏氧化膜的结构,加速铝制品的腐蚀。"
《提出问题》氯化钠溶液中的哪一种离子对氧化膜产生了破坏作用?
《实验方案》
| 实验序号 |
实验1 |
实验2 |
实验3 |
| 方案 |
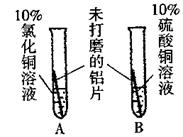 |
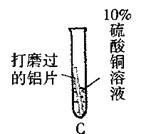 |
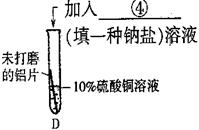 |
| 现象 |
A中铝片表面有红色固体析出;B中铝片无明显现象。 |
② |
与A中的现象相同 |
| 结论 |
溶液中对氧化膜产生了破坏作用的离子可能是 ①。 |
除去表面氧化膜的铝片会与CuSO4溶液反应。该反应的化学方程式③。 |
验证了实验1的结论。 |
《反思》针对实验3,莹莹认为还应增做一个对比实验,她的方案是向 试管中再加入 溶液,结果无明显现象。该实验可证明溶液中对氧化膜不产生破坏作用的离子是
⑤。
回收废旧干电池、保护环境是我们每个公民的义务,下面是我校化学兴趣小组探究回收废旧干电池意义的过程(片断),请帮助他们完成相应报告:
《提出问题》 废旧干电池的组成物质有什么?
《查阅资料》 1. 淀粉遇I2变蓝色 2. 部分酸碱盐溶解性表
  |
OH- |
NO3- |
Cl- |
SO42- |
CO32- |
| H+ |
 |
溶、挥 |
溶、挥 |
溶 |
溶、挥 |
| Ag+ |
 |
溶 |
不溶 |
微溶 |
不溶 |
| Ba2+ |
溶 |
溶 |
溶 |
不 溶 |
不 溶 |
《活动探究]》电池的内容物中有没有我们熟悉的离子?
《猜想1》 小组中某同学在剥开电池外壳时,闻到一股淡淡的刺激性气味,因此他猜想:电池的内容物中含有NH4+
《设计方案1]》取少量白色糊状物与混合、研磨,闻到氨味,证明上述猜想正确。
《猜想2》 可能含有OH-、CO32-、Cl-、SO42-中的一种或几种。
《设计方案2]》为了验证猜想2,设计如下实验,请完成表格中相应内容。
| 操作步骤 |
实验现象 |
相应的结论 |
| 1.取样。溶于适量的水,静置,过滤。取少量滤液,滴加紫色石蕊试液。 |
石蕊试液不变蓝色 |
没有存在 |
| 2.另取少量滤液,滴加过量的稀硝酸。 |
无明显现象 |
没有存在 |
| 3.向第2步所得溶液中滴加少量的硝酸钡溶液 |
没有SO42-存在 |
|
| 4.向第3步所得溶液中滴加少量硝酸银溶液 |
有白色沉淀产生 |
有存在 |
| 5.取白色糊状物,滴加少量碘液 |
则说明有淀粉存在 |
《结论》上述实验证明,电池内白色糊状物主要是(一种盐化学式)和淀粉等两种物质混合而成。
《交流与讨论]》根据上述探究过程,你认为电池内容物有无回收价值?请简要说明理由。
这学期,小亮和班级的两名同学主动承担了维护班级花坛的工作。前不久,他们发现有部分花的叶面出现了枯黄的现象,便及时向花坛里施用了足量的化肥,但效果并不明显。他们决定用所学的化学知识来解决这一问题。
(收集资料)
(1)花的叶色枯黄,他们选择施用_____________(填写“氮”、“磷”或“钾”)肥是正确的。
(2)前一段时间他们曾用熟石灰(化学式为_______________)对花坛中的___________性土壤进行过改良。
(3)近一个星期一直无雨,气温较高。
(4)通过查阅资料,小亮和同学们知道:含NH4+的盐受热或与碱混合会放出有刺激性气味的氨气,氨气的水溶液呈碱性。
(提出假设)
(1)太阳的曝晒和气温升高都可使肥效流失。
(2)熟石灰与化肥反应也可使肥效流失。
(设计并进行实验)
(1)小亮取少量这种化肥于试管中加热,并在试管口放一条干燥的pH试纸,pH试纸无变化。
(2)另取少量这种化肥与熟石灰混合,闻到____________气味。
[他的结论)由以上第二个实验中的现象他能得出肥效流失与_____________有关。
(反思与应用)
(1)小亮进行的第一个实验中,pH试纸无变化,这与查阅资料给出的信息不符,其原因是
。
(2)参与了小亮和同学们的探究活动,想必你也一定受到了启发,你能对小亮保存剩余化肥提出一条合理化建议吗?
下图是某小组同学验证质量守恒定律实验的片段。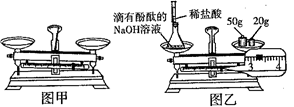
(1)如图甲所示,天平无法调节平衡。要使该天平平衡,应采取的措施;
(2)小明用图乙所示装置进行实验。反应前称得左盘内装置及物质总重量为 g,然后注入稀盐酸,充分反应后,能证明质量守恒定律的现象是;上述实验向氢氧化钠溶液中滴入酚酞的目的是,该反应的化学方程式为;
(3)小丽向氢氧化钠溶液中注入稀盐酸,发现有气泡产生,其原因是。
(6分)无土栽培是利用营养液栽培作物的一种方法.现有一种无色的营养液,可能由Ca(NO3)2、K2CO3、KCl 中的一种或几种物质组成.为探究其成分,某同学设计并完成了如下图所示的实验。
根据以上实验,请你回答:
由实验l可确定原营养液中一定没有的物质是(1)______________,理由是(2)____________
同学们将实验l所得混合物过滤后,对所得滤液成分进行了分析,请你与小组同学共同完成以下探究
<提出问题>滤液中的成分是什么?
<猜想与假设>小松同学:含有Ca(NO3)2NaNO3
小北同学含有KCl、Na2CO3、NaNO3
<表达与交流>结合对滤液成分的探究.同学们经过讨论确定了(3)________________同学猜想正确.理由是(4)________________:为了验证该同学的猜想,同学们向滤液中滴加适量的稀盐酸.没有观察到明显现象.从而否定了该同学的猜想.你认为滤液的成分可能为(5)________________________由此提示我们在分析反应后所得溶液中溶质的成分时应注意的问题是(6)________________________